Μεταστατικός καρκίνος του ήπατος εκ του παχέος εντέρου και του ορθού (ΜΝΗ-ΠΟ, MCRC)
Επιδημιολογία
Το ήπαρ είναι το πρώτο μείζον όργανο του σώματος, που μέσω της πυλαίας φλέβας δέχεται μεγάλη ποσότητα φλεβικού αίματος ανά λεπτό, ίσως δε αυτός είναι ο λόγος που αποτελεί την πιο συχνή εστία ανεύρεσης ηπατικών μεταστάσεων από κάθε όργανο της κοιλίας και ειδικά από ορθοκολικό καρκίνο.
Από όλα τα μεταστατικά καρκινώματα του ήπατος, εκείνο που ενδιαφέρει περισσότερο είναι αυτό εκ του παχέος εντέρου για πολλούς λόγους, ειδικά δε λόγω της πιθανότητας θεραπείας και ακόμα και ίασης μετά από ηπατεκτομή.
Τουλάχιστον 50.000 ασθενείς με καρκίνο του παχέος εντέρου αναπτύσσουν μεταστάσεις κάθε έτος στις ΗΠΑ, το δε 50% όλων των ασθενών με καρκίνο του παχέος εντέρου εμφανίζουν ή θα αναπτύξουν τελικά ηπατικές μεταστάσεις (στο 85% μέσα σε 2,5 έτη, και 100% μέσα σε 5 έτη). Στο 30% αυτών με μεταστατική νόσο του ήπατος (ΜΝΗ) από το παχύ έντερο και το ορθό, το ήπαρ είναι η μόνη περιοχή με μεταστάσεις.
Το 15-25% από τις μεταστάσεις αυτές ανιχνεύονται κατά τη διάγνωση της πρωτοπαθούς νόσου ή μέσα στους 3 πρώτους μήνες μετά την κολεκτομή (σύγχρονες), το δε 70% θα αναπτυχθούν ή ανιχνεύονται μετά τη θεραπεία της πρωτοπαθούς εστίας, συνήθως μέσα στα 3 πρώτα χρόνια μετά την κολεκτομή, και ονομάζονται μετάχρονες. Κατά συνέπεια, 10.000 έως 15.000 ασθενείς το χρόνο είναι υποψήφιοι για τοπική θεραπεία της ΜΝΗ από
ορθοκολικό καρκίνο στις ΗΠΑ.
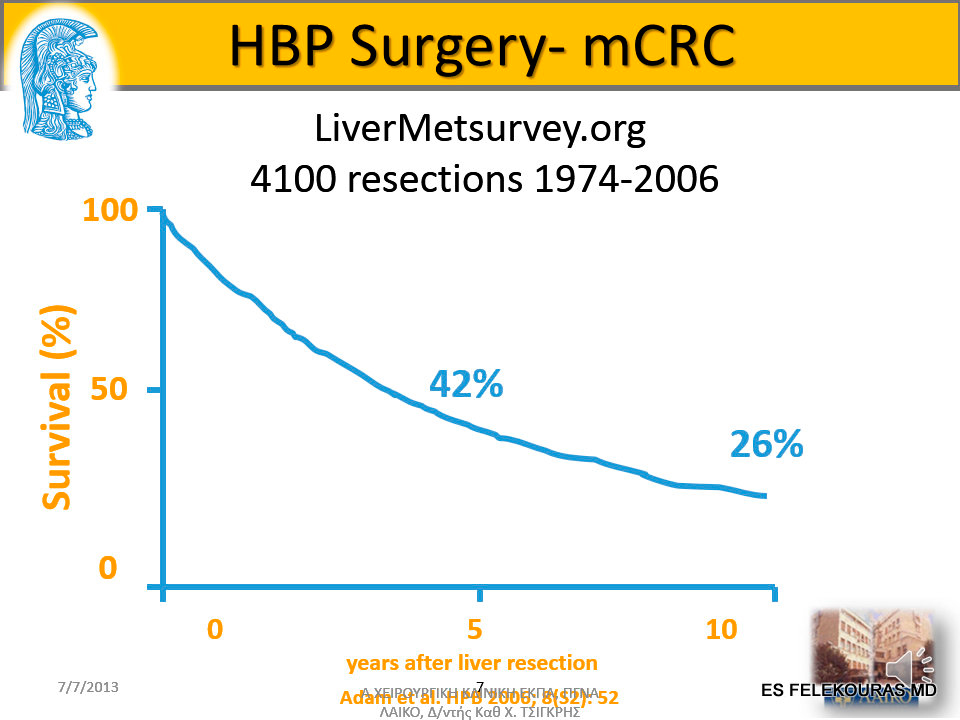
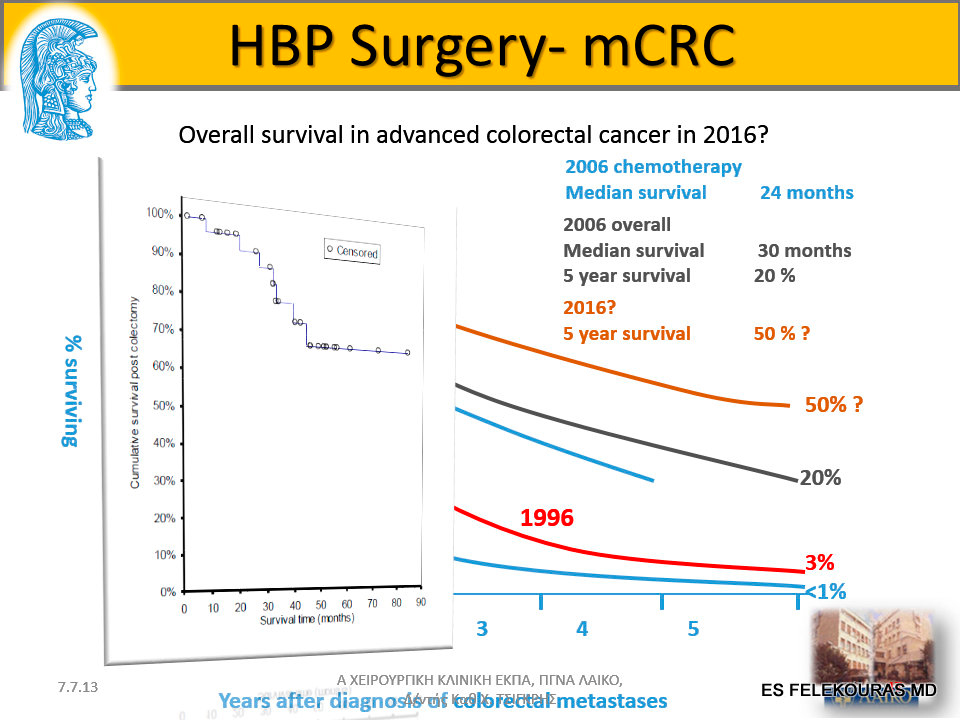
Χωρίς θεραπεία, η διάμεση επιβίωση των ασθενών με ΜΝΗ από ορθοκολικό καρκίνο είναι 6-9 μήνες, εξαρτώμενη κυρίως από την έκταση της νόσου κατά τη διάγνωση. Η ηπατεκτομή προσφέρει 5ετή επιβίωση 25-44%, πρόσφατα δε υπάρχουν αναφορές μέχρι και 58%, με περιεγχειρητική θνητότητα 0-6,6%. Ατυχώς, όμως, μόνο το 15-20% των ασθενών με ΜΝΗ από ορθοκολικό καρκίνο είναι κατάλληλοι για ηπατεκτομή, αν και με τις σύγχρονες θεραπευτικές μεθόδους αναμένεται να αυξηθεί το ποσοστό αυτό.
Κλινική εικόνα και διάγνωση
Λόγω του ότι η ανάπτυξη συμπτωματολογίας επισυμβαίνει αργά στην πορεία της νόσου, είναι απαραίτητη η πολύ στενή παρακολούθηση των ασθενών με κολεκτομή συνεπεία καρκίνου του παχέος εντέρου, με βιοχημικές εξετάσεις του ήπατος, CEA, υπερηχογράφημα (US) και αξονική τομογραφία (ΑΤ), ώστε να επιτευχθεί πρώιμη ανίχνευση πιθανών μεταστάσεων, ειδικά δε σε ασθενείς σταδίων Dukes Β και C. Το πρωτόκολλο
παρακολούθησης των ασθενών αυτών αλλάζει κατά περιόδους και αναλόγως των οικονομικών πόρων του συστήματος υγείας κάθε χώρας, αλλά οι εξαμηνιαίοι έλεγχοι ειδικά στα δύο πρώτα χρόνια μετά την κολεκτομή είναι πολύ σημαντικοί, ειδικά με υπερηχογράφημα ήπατος και κολονοσκόπιση, καθώς και διορθικό υπερηχογράφημα για τις χαμηλές πρόσθιες εκτομές.
Αύξηση του CEA κατά τη διάρκεια της πορείας του ασθενούς μετά από κολεκτομή, υποδεικνύει την ύπαρξη υποτροπής της νόσου. Η ανίχνευση της εστίας της υποτροπής της πάθησης θα πρέπει να γίνει με κάθε δυνατό μέσο. Έτσι, επίπεδα CEA >9 ng/ml σε συνδυασμό με θετικό US ή ΑΤ ή MRI ήπατος παρέχει ακρίβεια μέχρι και 98%. Αντίθετα, φυσιολογικό επίπεδο CEA σε συνδυασμό με αρνητικό US, αλλά κυρίως ΑΤ ή MRI ήπατος,
παρέχει ακρίβεια μέχρι και 95% όσον αφορά τον αποκλεισμό ΜΝΗ. Άλλοι συνδυασμοί εξετάσεων είναι λιγότερο ευαίσθητοι.
Από όλες τις ακτινολογικές εξετάσεις, οι εξελιγμένες ΑΤ (MDCT) και μαγνητικές τομογραφίες (MRI) θεωρούνται οι πιο αξιόπιστες με ακρίβεια 68%-92%, παρόλο που το US ήπατος με τη χρήση ενδοφλέβιων ενισχυτικών της ηχογένειας διαλυμάτων είναι μια πολλά υποσχόμενη εξέταση.
H αρχή της αιμάτωσης των ηπατικών μεταστάσεων, είναι ότι στην πλειονότητά τους λαμβάνουν αίμα από την ηπατική αρτηρία (εκτός από τα πολύ αρχικά στάδια, όπου η αποκλειστική τους αιμάτωση προέρχεται από την πυλαία κυκλοφορία, μιας και μέσω αυτής συνήθως γεννώνται) όπως και τα πρωτοπαθή νεοπλάσματα του ήπατος. Η MDCT που προοδευτικά αντικαθιστά όλες τις άλλες μορφές ΑΤ, παρέχει ίσως μεγαλύτερη ειδικότητα
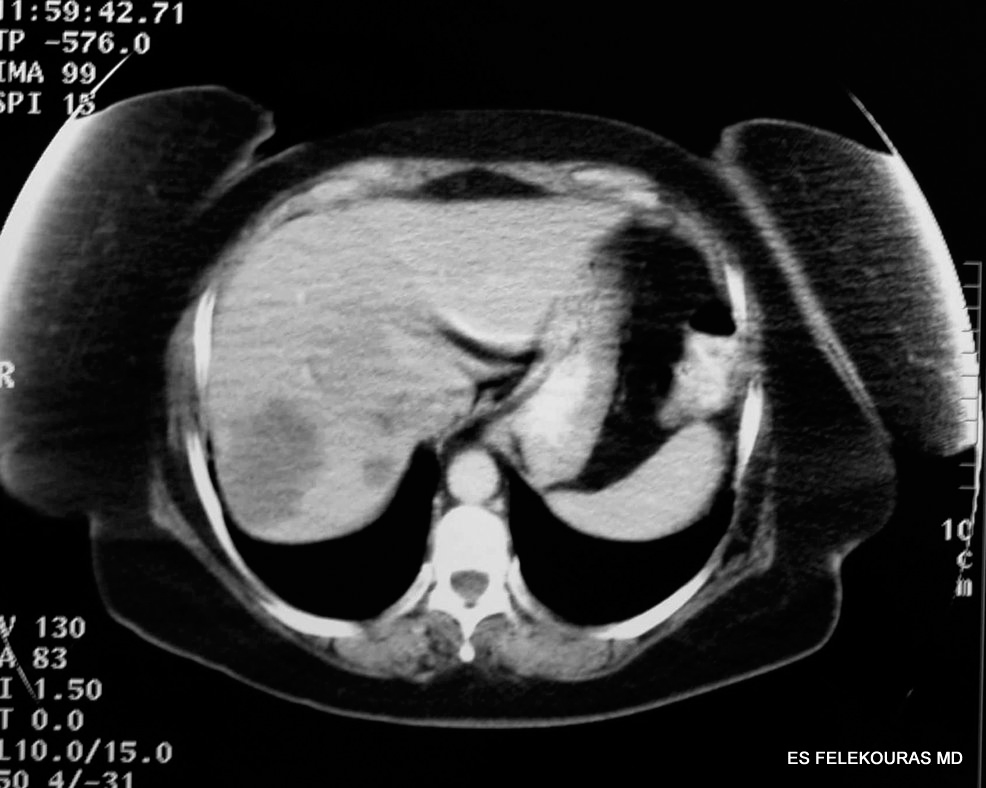
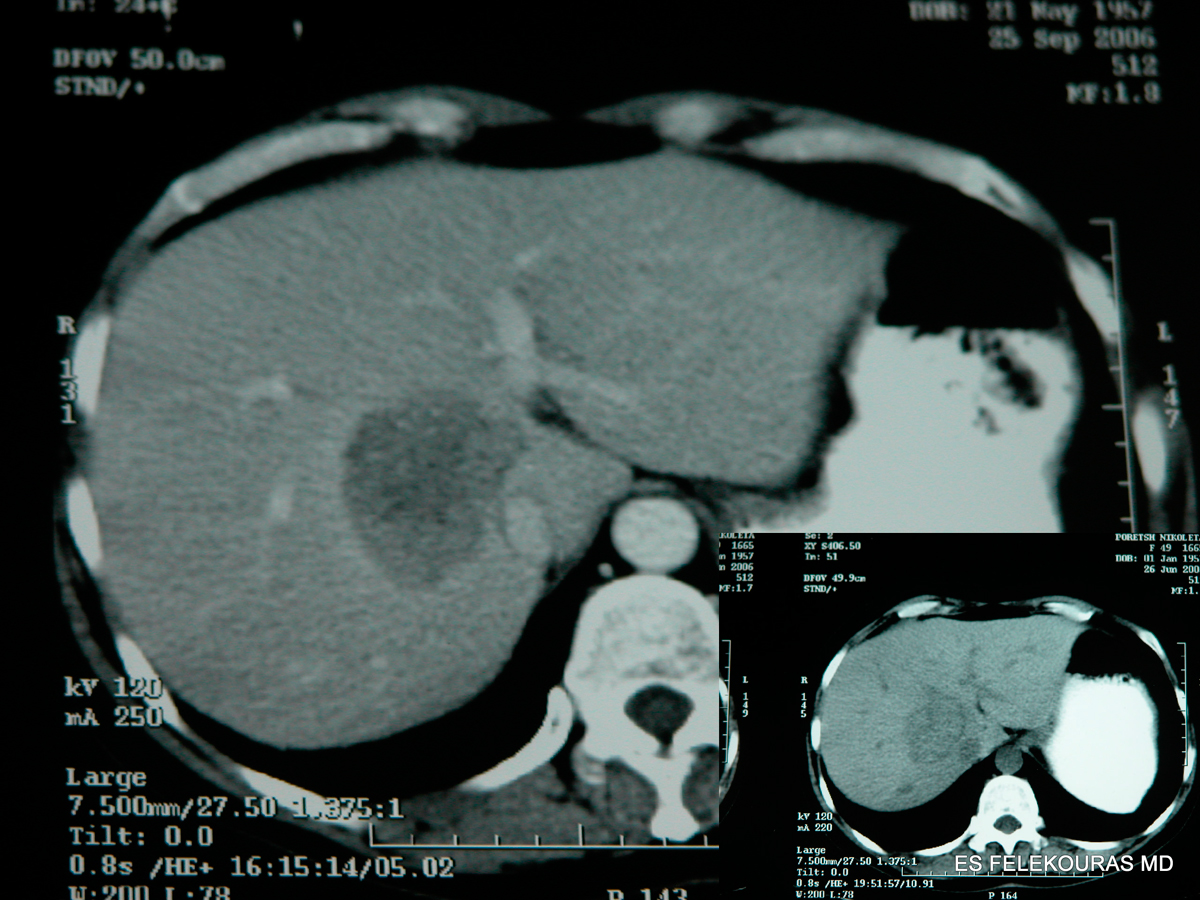
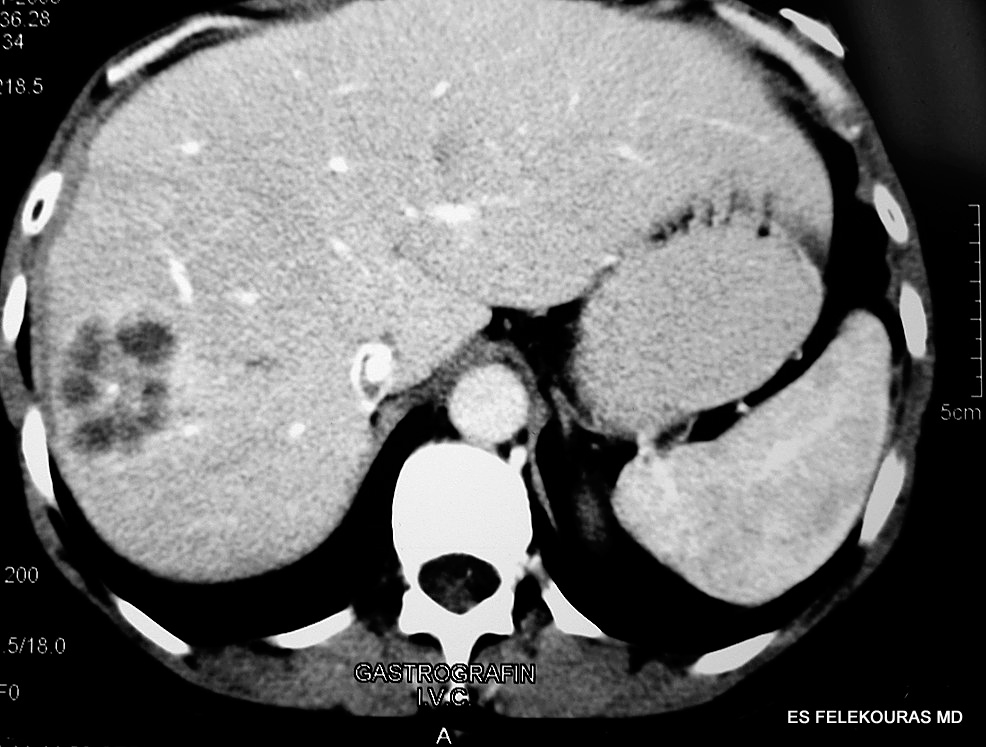
(specificity) στη διάκριση πρωτοπαθών και δευτεροπαθών όγκων του ήπατος. (εικόνα 1)
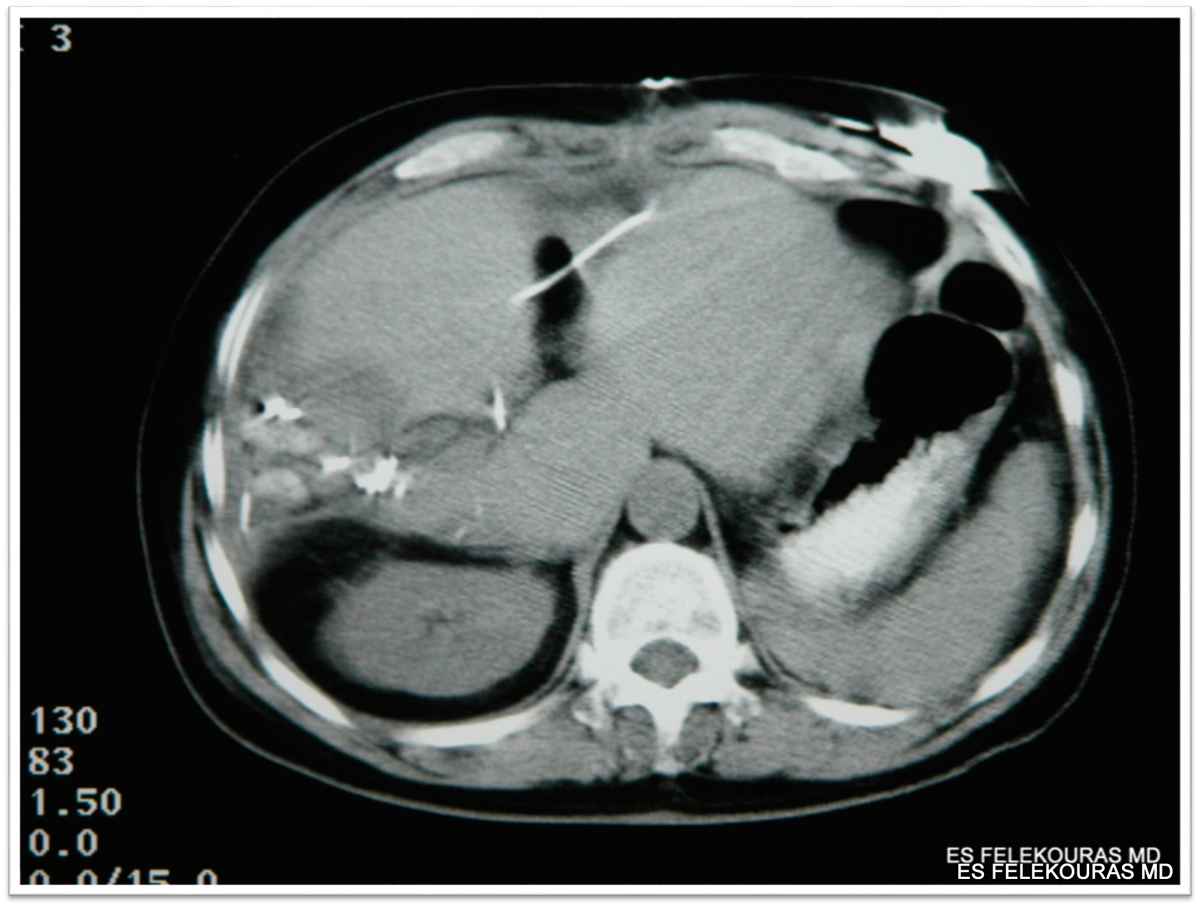
Εικόνα 1: Αξονική τομογραφία κοιλίας (CT) με χορήγηση ενδοφλεβίου και από του στόματος σκιαγραφικής ουσίας, σε ασθενή με μεταστατική νόσο του ήπατος από καρκίνο σιγμοειδούς. Διακρίνεται κατά την αρτηριακή φάση της εξέτασης η παρουσία μεταστατικών εστιών στο δεξιό λοβό του ήπατος.
Η MRI, συνεχίζει να είναι μια αξιόπιστη εναλλακτική λύση, που βελτιώνει τη διαγνωστική ακρίβεια και ειδικότητα σε συνδυασμό με τις προαναφερθείσες εξετάσεις. Αν και η ευαισθησία της MRI είναι περί το 64%, με την προσθήκη των σκιαγραφικών γαδολίνιο και ferumoxide έχει βελτιωθεί σημαντικά η ακρίβειά της, στην ανίχνευση των κακοήθων όγκων του ήπατος (80-90%) (εικόνα 2). Ο κύριος ρόλος της όμως είναι συμπληρωματικός για βλάβες που είναι δύσκολο να χαρακτηριστούν στην ΑΤ.
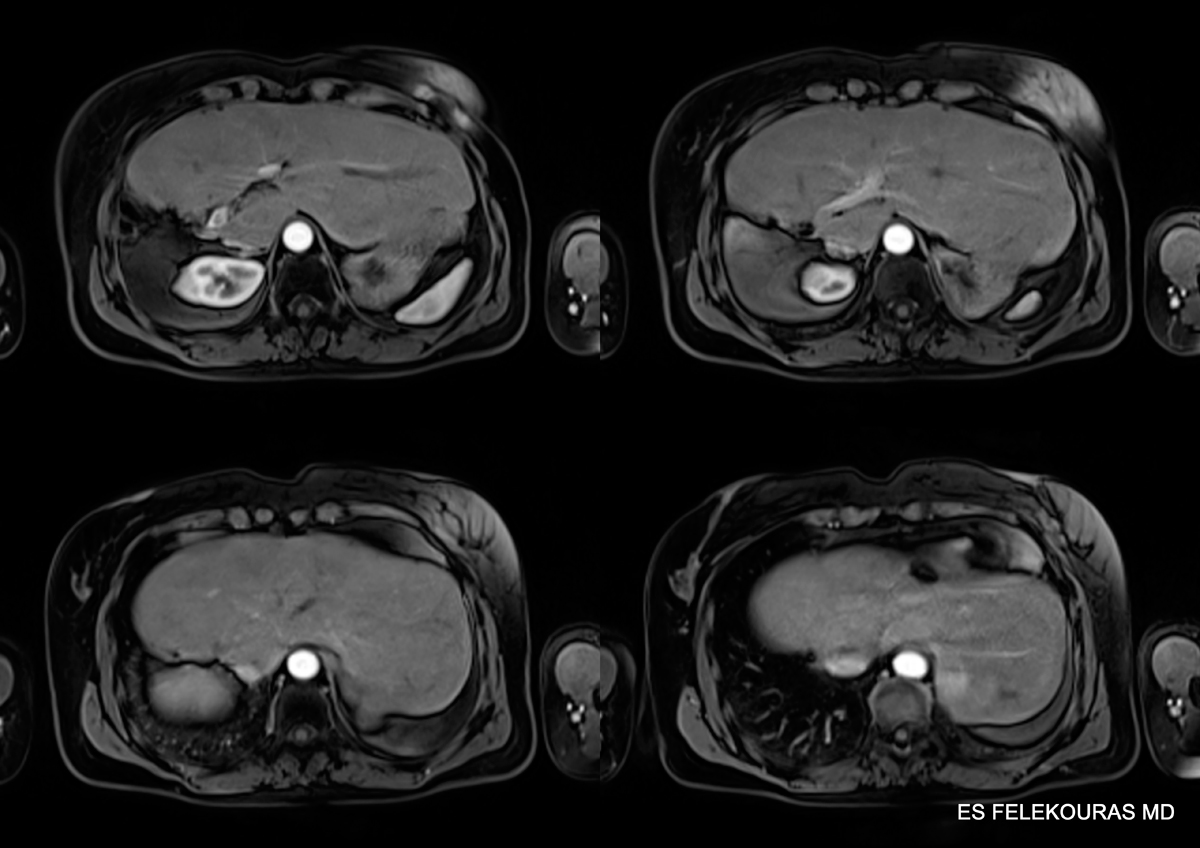
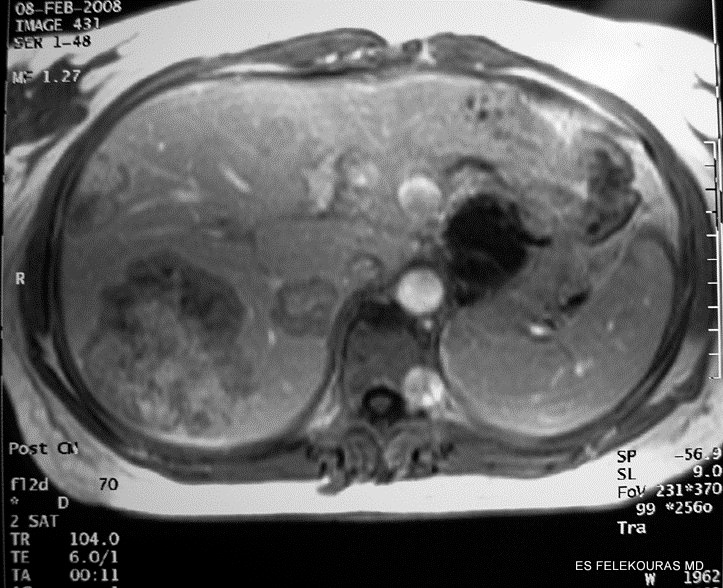
Εικόνα 2: Μαγνητική τομογραφία άνω κοιλίας (ΜRI) με χορήγηση ενδοφλεβίου παραμαγνητικής ουσίας σκιαγράφησης, σε ασθενή με μεταστατική νόσο του ήπατος από ορθοκολικό καρκίνο, όπου ευκρινώς αναδεικνύεται η μεταστατική βλάβη στο δεξιό λοβό του οργάνου αυτού.
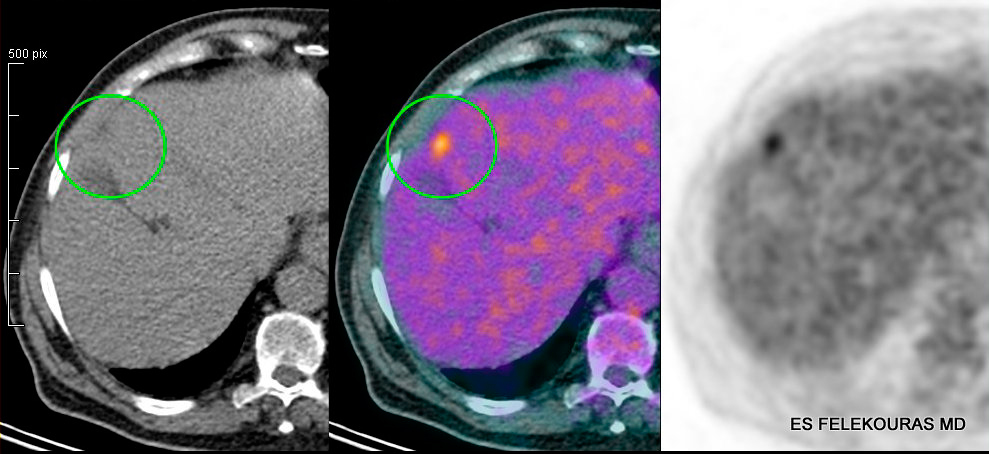
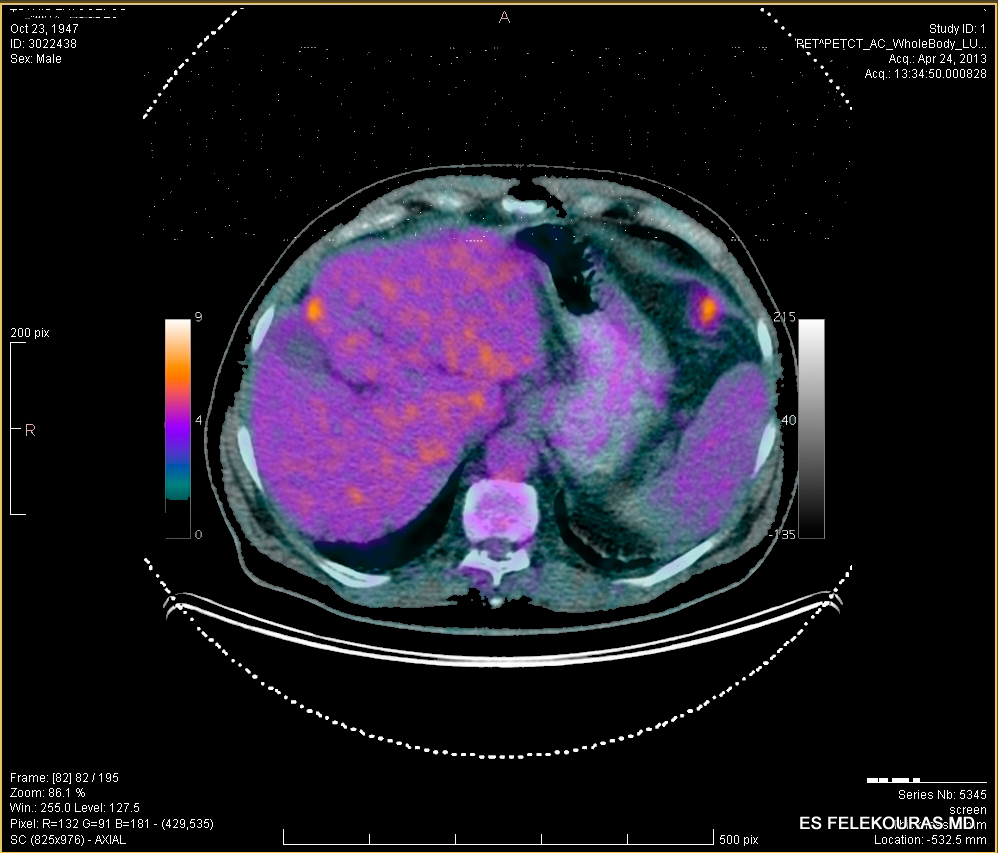
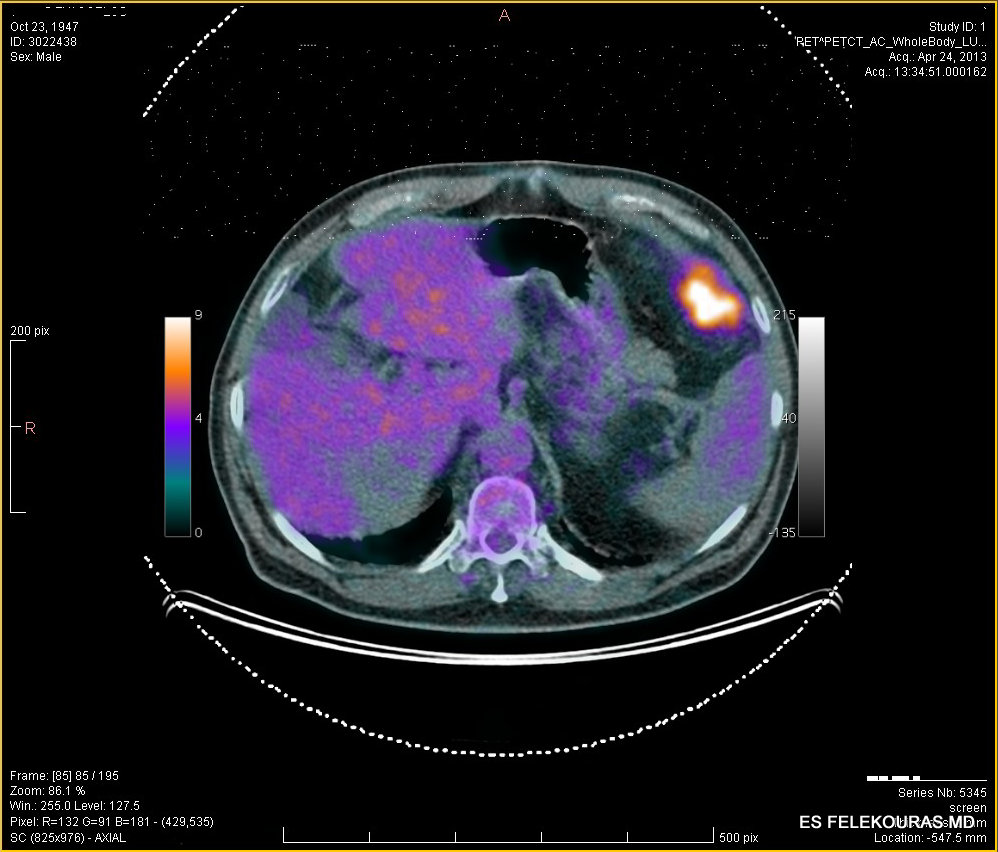
Η FDG-PET και το PEΤ/CT scan μπορεί να βοηθήσουν, εκεί που άλλες εξετάσεις δεν αναδεικνύουν την εστία της υποτροπής της νόσου, μπορεί δε να βελτιώσει την ανίχνευση και περαιτέρω εστιών, σε ασθενείς που υπεβλήθησαν στις άλλες κλασικές εξετάσεις κατά 25%. Η χρήση του FDG-PET για τη σταδιοποίηση της νόσου συνεχώς αυξάνεται πριν από τη θεραπεία της ΜΝΗ. Έτσι, μια μελέτη ανέδειξε ότι με την ανίχνευση των ανεγχείρητων
αυτών μεταστάσεων αποφεύγεται η ηπατεκτομή στο 25% και έτσι η 5ετής επιβίωση μπορεί να βελτιωθεί στο 58%, για ασθενείς που είχαν σταδιοποιηθεί με FDG-PET πριν την ηπατεκτομή. Για το λόγο αυτό, όταν είναι δυνατόν, πρέπει να εκτελεσθεί η PET/CT πριν τη χειρουργική θεραπεία και ιδιαίτερα πριν τη χημειοθεραπεία στους ασθενείς αυτούς. Η χημειοθεραπεία μπορεί να μετατρέψει τις μεταστατικές βλάβες σε λιγότερο ενεργές στην πρόσληψη της fluorodeoxyglucose (FDG) και έτσι να καταστήσει την εξέταση λιγότερο ευαίσθητη. Θα πρέπει να τονισθεί όμως, ότι η PET/CT και ειδικά η PET, δεν αποτελεί με κανένα τρόπο την εξέταση αυτή στην οποία θα βασίσουμε τις εγχειρητικές μας τεχνικές για την ηπατεκτομή, με τη βεβαιότητα δε ότι δεν είναι πιο ευαίσθητη από την MDCT, σε βλάβες μικρότερες από 1 cm ή σε βλεννώδεις όγκους (εικόνα 3).
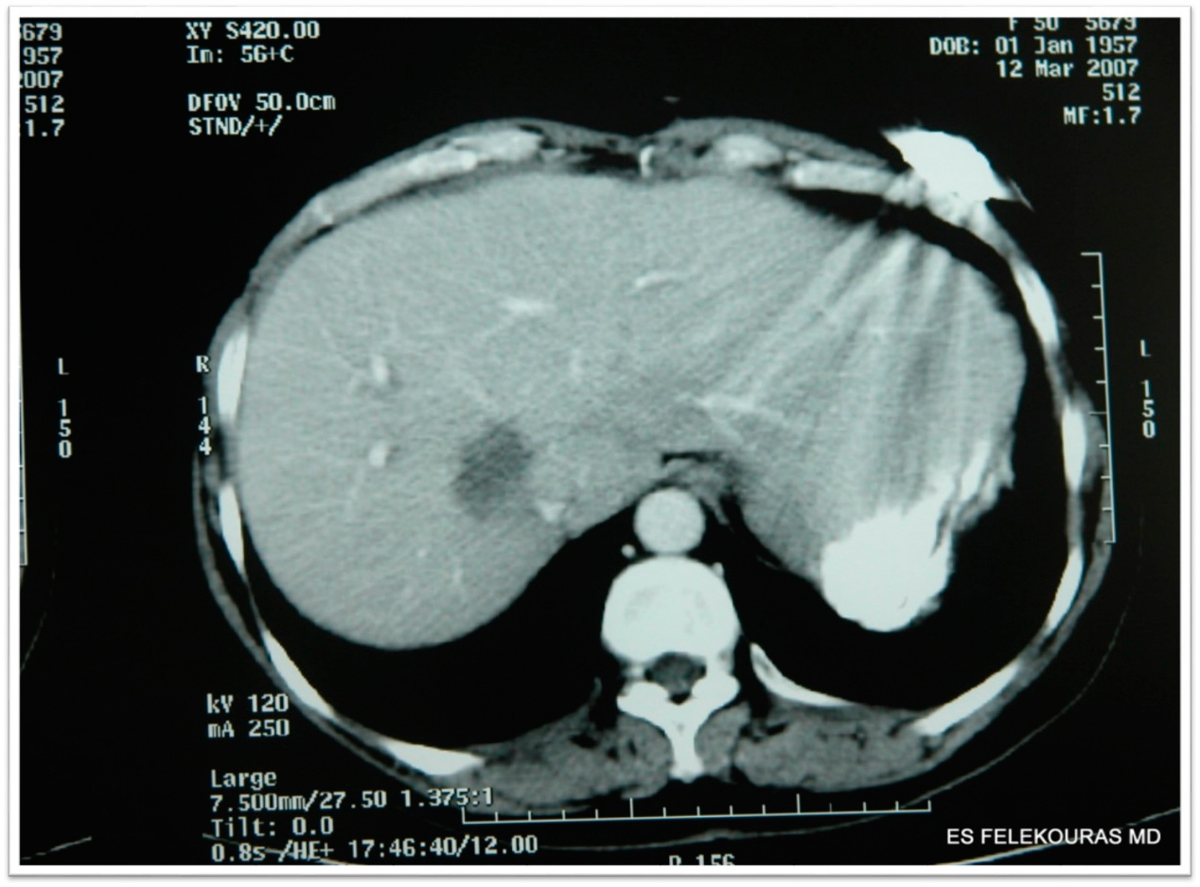
Εικόνα 3: Μεταστατική νόσος του ήπατος από καρκίνο του παχέος εντέρου σε ΑΤ και PET-CT και (κάτω) όπου αναδεικνύεται και άλλη εξωπεριτοναϊκή εστία στο αρ ημιδιάφραγμα.
Έτσι λοιπόν, παρόλο που η MDCT διαθέτει ευαισθησία πάνω από 90%, βλάβες μικρότερες από 1 cm δεν ανιχνεύονται συνήθως, όπως δεν ανιχνεύονται και οι εναποθέσεις στο περιτόναιο και στα διάφορα όργανα. Η MRI μπορεί να εμφανίσει μεγαλύτερη ακρίβεια στο ήπαρ από την ΑΤ, μια και χρησιμοποιεί ειδικά υλικά για σκιαγράφηση και αντίθεση, όπως τα παραμαγνητικά οξείδια του σιδήρου (SPIO), όμως δεν θεωρείται πιο ευαίσθητη στην εξωηπατική νόσο. Ο συνδυασμός όμως όλων των εξετάσεων ΑT, MRI και PET έχει αυξήσει την εξαιρεσιμότητα κατά 80%.
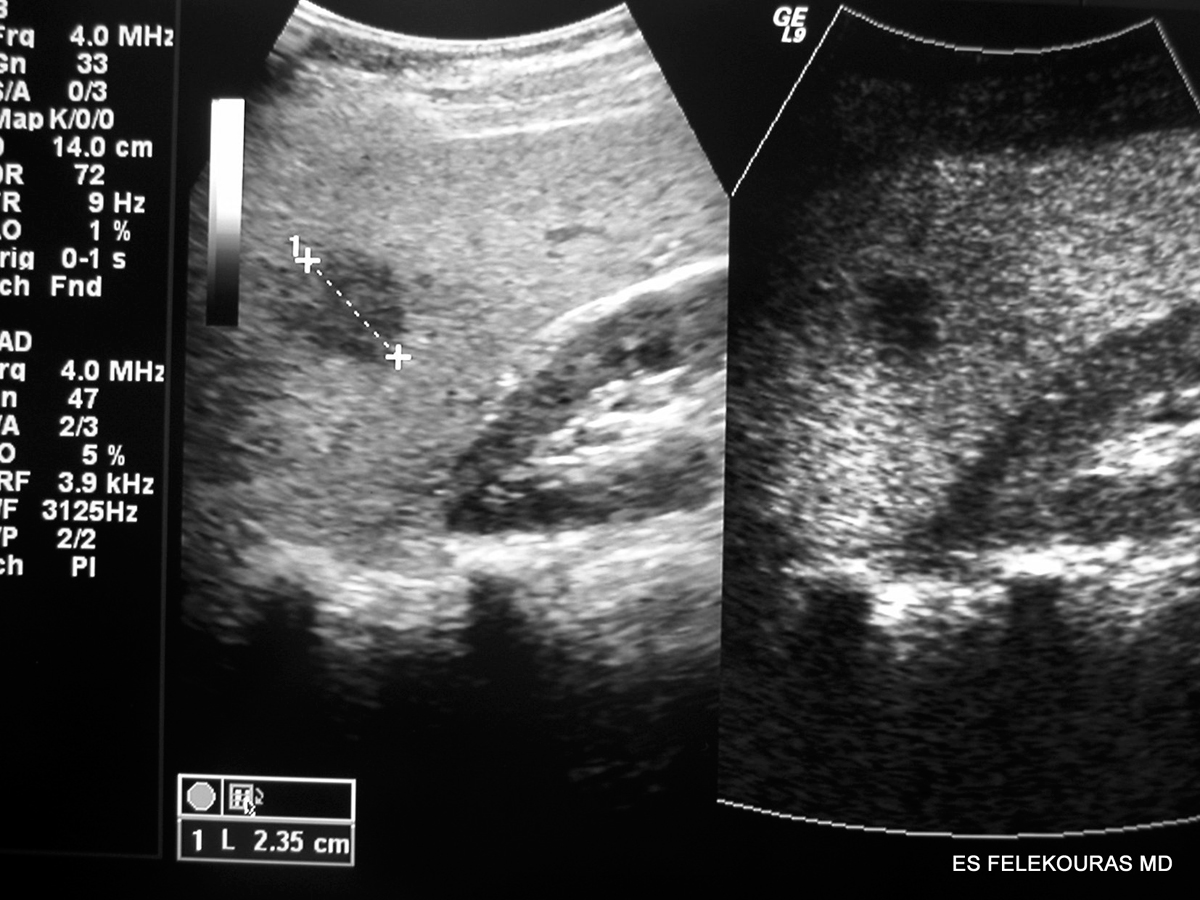
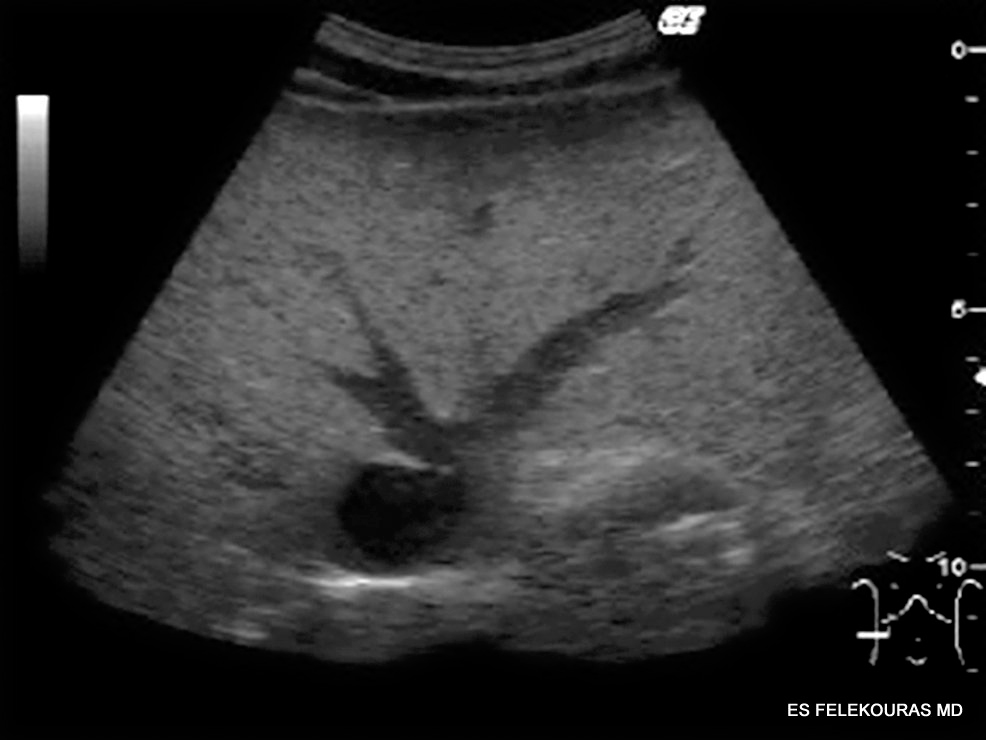
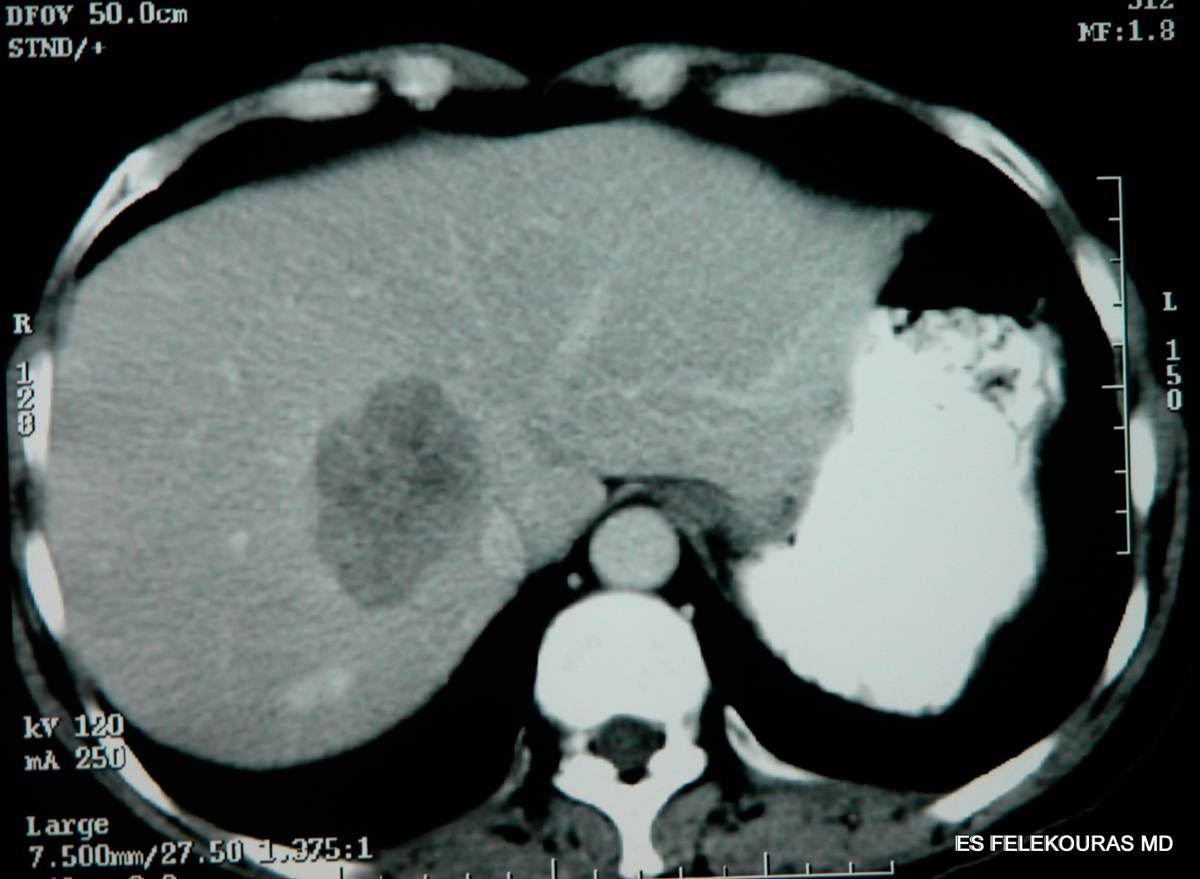
Το απλό υπερηχογράφημα ήπατος αν και είναι συνήθως η πρώτη εξέταση που κάνουμε στην υποψία της νόσου (εικόνα 4), ελάχιστα προσφέρει στην συνέχεια όμως το όμως το υπερηχογράφημα ήπατος με ενισχυτικά της ηχογένειας και το διεγχειρητικό US (IOUS) προσφέρουν τα μέγιστα στην διάγνωση και τον καθορισμό της θεραπείας των ασθενών με ΜΝΗ από κολοορθικό καρκίνο.
Εικόνα 4: Υπερηχογράφημα (US) ήπατος σε ασθενή με ΜΝΗ. Στην αριστερή αναπαράσταση διακρίνεται μετρήσιμη βλάβη 2,35 cm στο τμήμα VI του ήπατος. Η ίδια εικόνα με έντονους υποηχογενείς χαρακτήρες και στη δεξιά αναπαράσταση μετά από χορήγηση ενδοφλεβίου ουσίας μικροφυσαλλίδων (microbubble-contrast based US), η οποία συμβάλλει σημαντικά στην ανάδειξη μικρότερων εστιών με άτυπη/μεικτή υπερηχογραφική ηχογένεια, καθώς και στη διαφορική διάγνωση απεικονιστικών ευρημάτων του ήπατος.
Μια άλλη διαγνωστική επιλογή είναι η λαπαροσκόπηση και το διεγχειρητικό US (ΙΟUS, LIOUS). Το ΙΟUS θεωρείται η καλύτερη διαγνωστική επιλογή, μια και μπορεί να ανιχνεύει όζους μέχρι και 3-4 mm. Τα ευρήματα του IOUS φαίνεται ότι μπορεί να οδηγήσουν στην αλλαγή των θεραπευτικών χειρισμών μέχρι και στο 67% των περιπτώσεων (Εικόνα. 22.124, 22.125) ειδικά αν συνδυασθεί με ενισχυτικά της ηχογένειας.
Εικόνα 5: Απεικόνιση διεγχειρητικού υπερηχογραφήματος ήπατος (IOUS), όπου διακρίνεται η βασική ανατομία του απαγωγού αγγειακού δικτύου, στο ανατομικό επίπεδο της συμβολής των ηπατικών φλεβών με την ΚΚΦ.
Δεν χρειάζεται να γίνει βιοψία στις μεταστάσεις του ήπατος για να επιβεβαιωθεί η διάγνωση, μιας και οι εξετάσεις που διατίθενται είναι αρκετά ειδικές, και μόνο σε σπάνιες περιπτώσεις αυτή απαιτείται. Στην πραγματικότητα, η βιοψία μπορεί να είναι επιβλαβής, λόγω του κίνδυνου διασποράς του όγκου κατά μήκος της διαδρομής της βελόνας, γεγονός που έχει επιπτώσεις στην εξαιρεσιμότητα καθώς και στην απώτερη επιβίωση, ακόμα και όταν γίνει η ηπατεκτομή με συναφαίρεση της διαδρομής της βιοψίας.
Η προεγχειρητική απεικόνιση πρέπει να καθορίσει τον αριθμό των μεταστάσεων, την κατανομή και την εγγύτητά τους με σημαντικές χοληφόρες και αγγειακές δομές. Η ΑΤ μπορεί με ένα υψηλό βαθμό ευαισθησίας να αποκλείσει πνευμονικές μεταστάσεις, ενδείκνυται δε στις περισσότερες περιπτώσεις, αν και η α/α θώρακος μόνον, είναι αρκετή στην πλειονότητα των ασθενών. Μελέτες ευρίσκονται εν εξελίξει για να αξιολογήσουν το πιθανό προσθετό όφελος του ελέγχου με PET, στην ανίχνευση εξωηπατικής νόσου και απομακρυσμένων μεταστάσεων. Η διαγνωστική λαπαροσκόπηση πριν από την οριστική λαπαροτομία θα μπορούσε να βοηθήσει στην αξιολόγηση της έκτασης της νόσου και έτσι να αποφευχθεί αυτή σε ένα 10-25% των ασθενών, χρησιμοποιούμενη επιλεκτικά.
Εντούτοις, με τις όλο και περισσότερο ευαίσθητες προεγχειρητικές τεχνικές απεικόνισης, συμπεριλαμβανομένων των PET/CT, και με την αυξανόμενη χρήση της καταστροφής εστιών με RFA και της εξαίρεσης εξωηπατικών εστιών, λιγότεροι ασθενείς υποβάλλονται σε μη θεραπευτική λαπαροτομία, ακόμη και χωρίς προγενέστερη λαπαροσκόπηση. Έτσι, η απλή προεγχειρητική σταδιοποίηση επιτυγχάνεται κυρίως με ΑΤ, παρόλο που είναι δύσκολη η ανίχνευση μεταστάσεων κάτω από 1 cm.
Συνοπτικά, λοιπόν, όταν κατά τη διάρκεια της μετεγχειρητικής παρακολούθησης ένας ασθενής παρουσιάζει ΜΝΗ, είναι υποψήφιος για χειρουργική θεραπεία, ενώ ο πλήρης έλεγχός του είναι επιτακτικός. Η κολονοσκόπιση είναι επίσης απαραίτητη εάν δεν έχει γίνει κατά τη διάρκεια του τελευταίου έτους, για να αποκλεισθεί η τοπική αναστομωτική υποτροπή, καθώς και σύγχρονες ή μετάχρονες καρκινικές βλάβες στο παχύ έντερο. Ο πλήρης έλεγχος της κοιλίας κυρίως με ΑΤ, και σπάνια με MRI είναι απαραίτητος.
Χειρουργική θεραπεία
Οι θεραπευτικές επιλογές που έχουμε για ασθενείς με ΜΝΗ από ορθοκολικό καρκίνο είναι αρκετές (εικόνα 6). Από αυτές η μόνη δυνητικά θεραπευτική είναι η ηπατεκτομή με επιβίωση 20ετίας περί το 20%, μιας και οι ασθενείς που υπεβλήθησαν μόνο σε συστηματική χημειοθεραπεία (στην πλέον σύγχρονη) εμφανίζουν μέση επιβίωση περίπου 2 χρόνια.
Εικόνα 6: Επιλογές θεραπείας σε ασθενή με ΜΝΗ-ΚΟ
Αναλυτικότερα οι σύγχρονες θεραπευτικές επιλογές στο μεταστατικό καρκίνο του ήπατος από το παχύ έντερο είναι:
- Χειρουργική εξαίρεση (ηπατεκτομή)
- Συστηματική χημειοθεραπεία
- Περιοχική χημειοθεραπεία (hepatic artery infusion pump, HAI)
- Προεγχειρητική συστηματική χημειοθεραπεία (neoadjuvant)
- Μετεγχειρητική συστηματική χημειοθεραπεία (adjuvant)
- Θερμική καταστροφή
– RF (radiofrequency ablation)
– Άλλες μέθοδοι (όπως κρυοθεραπεία, μικροκύματα κ.ά.) - Εκλεκτική εσωτερική ακτινοθεραπεία (Selective internal radiotherapy, SIRT)
- Χημειοεμβολισμός
- Ανοσοθεραπεία
- ΣΥΝΔΥΑΣΜΟΣ
Εκτίμηση ασθενούς με ΜΝΗ από καρκίνο του παχέος εντέρου
Σταδιοποίηση, ενδείξεις και κριτήρια εξαιρεσιμότητας
Είναι σαφές ότι η επιλογή των ασθενών προς ηπατεκτομή είναι θεμελιώδους σημασίας για την επίτευξη καλών αποτελεσμάτων. Αν και τα κριτήρια επιλογής ασθενών με ΜΝΗ από το παχύ έντερο για ηπατεκτομή έχουν επεκταθεί κατά τη διάρκεια των τελευταίων 2 δεκαετιών, τα ειδικά κριτήρια για την επιλογή τους παραμένουν αμφισβητούμενα. Το κύριο ερώτημα είναι το μέγεθος της ηπατεκτομής σε συγκεκριμένο ασθενή. Η απάντηση στο
ερώτημα αυτό πρώτα από όλα προέρχεται από την εκτίμηση της λειτουργικότητας του πατος όπως αυτή εκφράζεται κυρίως από το σύστημα Child-Pugh, το επίπεδο του ικτέρου, και την ογκομέτρηση του ήπατος (CT volumetry).
Με τη βελτίωση των χειρουργικών μεθόδων, οι ενδείξεις για ηπατεκτομή έχουν τα τελευταία χρόνια αλλάξει, ενώ τα κριτήρια του Ekberg (1986) έχουν τροποποιηθεί. Η ηπατεκτομή με τα κριτήρια αυτά προσέφερε 5ετή επιβίωση 25%, όταν χωρίς ηπατεκτομή οι ασθενείς αυτοί δεν είχαν καμία τύχη (5 ετή επιβίωση 2%). Τα κριτήρια αυτά απεδείχθησαν πολύ αυστηρά, έτσι ώστε σήμερα να ακολουθούνται πιο φιλελεύθερες απόψεις. Ο μεγάλος αριθμός των ηπατικών μεταστάσεων δεν αποτελεί πλέον αντένδειξη (είναι όμως κακό προγνωστικό σημείο), ομοίως δε, η επέκταση της ΜΝΗ σε παρακείμενες ανατομικές δομές και η τοπική ή περιοχική υποτροπή του αρχικού καρκίνου δεν συνιστούν αντενδείξεις για ηπατεκτομή.
Η American Hepato-Pancreato-Biliary Association σε Consensus Conference του 2006, συνέστησε ότι η ΜΝΗ από ορθοκολικό καρκίνο πρέπει να θεωρείται εξαιρέσιμη αν:
- Είναι δυνατή η πλήρης εκτομή (R ).
- Αν δύο (2) εν συνεχεία τμήματα του ήπατος μπορεί να παραμείνουν με πλήρη προσαγωγά και απαγωγά αγγεία και χολαγγεία.
- Αν ο όγκος του εναπομείναντος ήπατος (FLR) είναι επαρκής και λειτουργικός (>20% του συνολικού όγκου του ήπατος σε φυσιολογικό ήπαρ).
Φυσικά υπάρχουν και αντενδείξεις για την ηπατεκτομή σε ΜΝΗ-ΚΟ
- Όχι όταν ριζική επέμβαση (R0) δεν μπορεί να γίνει (αρκετές φορές παραβλέπεται και όχι άδικα μια και οι ασθενείς που έχουν R1 εκτομή έχουν που καλό προσδόκιμο επιβίωσης )
- Λεμφαδενική διασπορά στον ηπατοδωδεκαδακτυλικό σύνδεσμο ή κατά μήκος της ΗΑ και του αλληρείου τρίποδα (σήμερα αμφισβητείται)
- Εξωηπατική νόσος (σήμερα αμφισβητείται)
- Προχωρημένη κίρρωση
- Ίκτερος, εκτός από όταν οφείλεται σε διήθηση ή έμβολο εντός του χοληδόχου ή ηπατικού πόρου (πολλές φορές παραβλέπεται)
- Εξαιρέσεις
a. η τοπικά εκτεινόμενη νόσος που μπορεί να εξαιρεθεί μαζί με τον όγκο του ήπατος (en bloc)
b. η εξαιρέσιμη μεταστατική νόσος του πνεύμονα
c. εξαιρέσιμη τοπική υποτροπή της πρωτοπαθούς εστίας στο παχύ έντερο
d. εξαιρέσιμη λεμφαδενική διασπορά στον ηπατοδωδεκαδακτυλικό σύνδεσμο
e. μερική εκτομή (cytoreductive surgery), περιστασιακά σε ασθενείς με συμπωματική ΜΝΗ
Όσον αφορά τα κριτήρια εξαιρεσιμότητας, η εμπειρία έδειξε ότι, οι ασθενείς με τους παραδοσιακούς κακούς προγνωστικούς παράγοντες μπορούν να έχουν καλύτερη επιβίωση μετά ηπατεκτομή από ότι θεωρούνταν. Έτσι, τα τελευταία χρόνια, τα κριτήρια αυτά άλλαξαν από μορφολογικά σε παθολογοανατομικά, βασισμένα στην ιδέα της R0 εκτομής (μικροσκοπικά υγιή όρια).
Εικόνα 7: Μη αμφισβητούμενα προς το παρόν αξιώματα της θεραπείας της ΜΝΗ-ΚΟ
Προγνωστικοί παράγοντες
Οι παραδοσιακοί παράγοντες που πιο στενά συνδέονται με πτωχή έκβαση μετά από ηπατεκτομή για ΜΝΗ από το παχύ έντερο είναι τα θετικά όρια εκτομής και η εξωηπατική νόσος κατά την ηπατεκτομή.
Στην πορεία του χρόνου και στην προσπάθεια επίτευξης ενός πιο ακριβούς προγνωστικού συστήματος προεγχειρητικής αξιολόγησης και επιλογής των ασθενών για ηπατεκτομή, διάφοροι προγνωστικοί παράγοντες ερευνήθηκαν και αξιολογήθηκαν σε μεγάλες σειρές ασθενών με ΜΝΗ. Πολλοί τελικά βρέθηκαν να είναι οι αρνητικοί προγνωστικοί παράγοντες, που με διαφορετικό κάθε φορά τρόπο επηρεάζουν την επιβίωση των ασθενών μετά από
ηπατεκτομή για ΜΝΗ εκ του παχέος εντέρου. Οι σημαντικότεροι εξ αυτών κατά σειρά σπουδαιότητάς τους είναι οι ακόλουθοι:
- Εξωηπατική νόσος
- Τα θετικά ιστολογικά όρια εκτομής (όριο εκτομής >1 cm, αμφισβητείται έντονα)
- Μετάγγιση αίματος περιεγχειρητικά (άρα σκοπός μας είναι η αναίμακτη χειρουργική)
- Θετικοί λεμφαδένες στον ηπατοδωδεκαδακτυλικό σύνδεσμο
- >1 όζος και γενικά ο αριθμός των ηπατικών μεταστάσεων, όπως και η κατανομή τους (αν και έχει βρεθεί ότι εξαίρεση μέχρι και 8 όζων, προσδίδει την ίδια περίπου επιβίωση με αυτή της εξαίρεσης ενός όζου, εφόσον η ηπατεκτομή μας είναι R0)
- Επίπεδο CEA >200 ng/ml κατά την ηπατεκτομή
- Μέγεθος του όγκου >5 cm (όσο μεγαλύτερο τόσο πιο δυσμενής η πρόγνωση)
- Διάστημα ελεύθερο νόσου, μετά κολεκτομή <12 μήνες
- Πρωτοπαθής νόσος (ορθοκολικός καρκίνος) με θετικούς λεμφαδένες
- Διαφοροποίηση του πρωτοπαθούς όγκου
- Ηλικία >70 έτη
- Κακή γενική κατάσταση
Αυτοί οι ως άνω παράγοντες αναδείχθηκαν από την μελέτη των Fong και συν., από το Memorial Sloan-Kettering Cancer Center (MSKCC, USA), και έχουν αναδειχτεί ως προγνωστικοί παράγοντες και έχουν δημιουργηθεί αντίστοιχα συστήματα που χρησιμοποιούν τους αρνητικούς προγνωστικούς παράγοντες που προέκυψαν από τη μελέτη αυτή, ενώ παράλληλα αναπτύχθηκε ένα προγνωστικό σύστημα που προβλέπει και την επιβίωση.
Οι παράγοντες αυτοί βοήθησαν στο να επιλεγούν ασθενείς προς ηπατεκτομή με μεγαλύτερη βεβαιότητα ως προς το καλό απώτερο αποτέλεσμα. Αξιοσημείωτο είναι το γεγονός ότι οι περισσότεροι από αυτούς τους παράγοντες θεωρούνται από πολλούς ως αντενδείξεις (σχετικές και απόλυτες) για ηπατεκτομή που όμως είναι λάθος μια και είναι απλώς προγνωστικοί παράγοντες. Παρόλα αυτά, πιο σύγχρονες μελέτες θεωρούν ότι κυρίως η μετάγγιση αίματος περιεγχειρητικά και οι θετικοί λεμφαδένες στον ηπατοδωδεκαδακτυλικό σύνδεσμο αποτελούν τους μείζονες παράγοντες που καθορίζουν την επιβίωση και την υποτροπή.
Παρόλα τα συστήματα αξιολόγησης, που με τη χρήση διαφόρων παραγόντων είναι επιστημονικά τεκμηριωμένα, η γενική εφαρμογή και χρησιμότητά τους πέραν των μεγάλων κέντρων αναφοράς δεν έχει επιβεβαιωθεί από άλλες 11 τουλάχιστον μελέτες σε άλλα μεγάλα κέντρα. Έτσι, σήμερα δεν υπάρχει κανένα απόλυτα αξιόπιστο σύστημα για την επιλογή ασθενών με ΜΝΗ προς ηπατεκτομή, του οποίου η εφαρμογή να προτείνεται ανεπιφύλακτα και να αποτελεί το βασικό κανόνα προεπιλογής.
Πιθανότατα η μελλοντική ανάπτυξη άλλων προγνωστικών συστημάτων που θα περιλαμβάνουν ακόμα πιο πολλά στοιχεία, όπως μεγαλύτερες ομάδες ασθενών, γενετικούς δείκτες κ.λπ. να φανούν περισσότερο.
Τα στοιχεία αυτά χρησιμεύουν κυρίως για να υπογραμμίσουν ότι οι παραδοσιακοί προεγχειρητικοί κλινικοπαθολογικοί προγνωστικοί παράγοντες μπορούν να θεωρούνται γενικά ωφέλιμοι, αλλά παράλληλα είναι και ανεπαρκείς στο να καθορίσουν την αληθινή βιολογική συμπεριφορά των ορθοκολικών μεταστάσεων, δεν θα πρέπει δε να χρησιμοποιηθούν για να αποκλείσουν ασθενείς από τη χειρουργική εκτίμηση.
Θεωρητικά, δεν υπάρχουν απόλυτες αντενδείξεις για ηπατεκτομή σε ασθενείς με ΜΝΗ από ορθοκολικό καρκίνο, αλλά πρακτικά η ύπαρξη μη εξαιρέσιμης εξωηπατικής νόσου και η αδυναμία εξαίρεσης όλης της ΜΝΗ (αδυναμία τουλάχιστον R1 εκτομής) είναι σχεδόν απόλυτες αντενδείξεις για ηπατεκτομή. Εξαίρεση στον κανόνα αυτό αποτελεί κυρίως η ύπαρξη εξαιρέσιμης μεταστατικής νόσου στον πνεύμονα και η εξαιρέσιμη τοπική υποτροπή της πρωτοπαθούς εστίας στο παχύ έντερο.
Συμπερασματικά, όλοι οι ασθενείς με ΜΝΗ που κρίνεται ότι είναι χειρουργήσιμοι, ανεξαρτήτως των σχετικών κλινικοπαθολογικών παραγόντων, πρέπει να θεωρηθούν ως πιθανοί υποψήφιοι χειρουργικής αντιμετώπισης, μιας και η ηπατεκτομή παραμένει η πρέπουσα λύση, εφ’ όσον μπορεί να είναι πλήρης (R0 η τουλάχιστον R1) και σε όσους ασθενείς μπορεί να επιτευχθεί.
Ηπατεκτομή
Η ηπατεκτομή είναι η μόνη μορφή θεραπείας που προσφέρει 5ετή απώτερη επιβίωση για τους ασθενείς με ΜΝΗ από ορθοκολικό καρκίνο, που κυμαίνεται από 25-58%. Το είδος της ηπατεκτομής που θα εκτελεσθεί για να επιτευχθεί το προσδοκώμενο αποτέλεσμα, είναι βασικά συνάρτηση του σταδίου της νόσου ποικίλλει δε από απλή τμηματεκτομή ή άτυπη εκτομή μέχρι δεξιά η αριστερή τριτμηματεκτομή, όπως και στο ΗΚΚ (Εικόνα. 22.130).
Ακόμη σήμερα αυτός ο κυρίαρχος ρόλος της R0 εκτομής με μεγάλες επεμβάσεις και εκτεταμένες ηπατεκτομές θεωρείται ξεπερασμένος και οι επεμβάσεις διατήρησης του ηπατικού παρεγχύματος (Liver parenchymal preserving surgery) είναι η πρώτη μας επιλογή με σκοπό να διατηρήσουμε όσο το δυνατόν περισσότερο ηπατικό παρέγχυμα για το μέλλον αυτών των ασθενών στα πλαίσια βέβαια πάντα μιας R0 εκτομής.
Εικόνα 8: Δεξιά εκτεταμένη ηπατεκτομή με σύγχρονη κολεκτομή για ΜΝΗ. Επάνω η ΑΤ του ασθενούς
Η αξία της ηπατεκτομής στη θεραπεία της ΜΝΗ από ορθοκολικό καρκίνο δεν έχει ποτέ αποδειχθεί με μια τυπική προοπτική τυφλή μελέτη, μιας και θεωρείται ότι δεν είναι ηθικά σωστό να αρνηθεί κανείς τη χειρουργική θεραπεία σε ασθενείς με εξαιρέσιμες ηπατικές μεταστάσεις.
Ο οδικός χάρτης για την ηπατεκτομή
Για να φθάσει όμως κάποιος στην ηπατεκτομή πρέπει να σχεδιάσει την θεραπεία και την επέμβαση πολύ προσεκτικά με συνέπεια να είναι απαραίτητο να μελετηθούν όλα τα στοιχεία που διατίθενται από τον προεγχειρητικό έλεγχο, όπως ο αριθμός των μεταστάσεων, η ύπαρξη μεταστάσεων σε άλλο όργανο, η δυνατότητα επίτευξης αρνητικών ορίων εκτομής κ.ά. Ο χάρτης για την ηπατεκτομή είναι τόσο σημαντικός που θα πρέπει να αποφασισθεί από ομάδα πολύ εξειδικευμένων ιατρών, πάντα με τη σκέψη της θεραπείας και όχι μόνο της παράτασης της ζωής του ασθενούς. Οι ιατροί αυτοί είναι ο χειρουργός ήπατος, ο ογκολόγος, ο επεμβατικός ακτινολόγος κ.λπ. Μόνο έτσι είναι δυνατόν να επιτευχθούν τα αναμενόμενα αποτελέσματα.
Η σταδιοποίηση της ΜΝΗ, τα κριτήρια εξαιρεσιμότητας και οι παράγοντες που συνδέονται με την πρόγνωση των ασθενών αποτελούν παραμέτρους, που προσεγγίστηκαν αναλυτικά στην αναφορά για την επιλογή και την προεγχειρητική εκτίμηση των προς ηπατεκτομή για ΜΝΗ αρρώστων.
Συνοπτικά, υπάρχουν μερικά σύγχρονα αξιώματα στη χειρουργική της ΜΝΗ από ορθοκολικό καρκίνο, που συνήθως ακολουθούνται από όλους.
Συγκεκριμένα:
- Η ηπατεκτομή προτιμάται πάντα από τις τοπικές στρατηγικές καταστροφής του όγκου (RFA, Cryo- ablation κ.λπ.).
- Η ηπατεκτομή αντενδείκνυται απολύτως, όταν υπάρχει:
a. μη εξαιρέσιμη εξωηπατική νόσος
b. εκτεταμένη συμμετοχή του ήπατος (>70%, περισσότερα από 6 τμήματα, ή συμμετοχή και των τριών ηπατικών φλεβών αλλά το τελευταίο αμφισβητείται σε πολύ μεγάλα κέντρα)
c. σημαντική ηπατική ανεπάρκεια
d. κακή γενική κατάσταση (υψηλό ASA και APΑCHE). - Μετά από ηπατεκτομή πρέπει να ακολουθήσει και μετεγχειρητική χημειοθεραπεία.
Παράγοντες που δεν επηρεάζουν τη στρατηγική της χειρουργικής θεραπείας είναι:
- Η ηλικία
- Το αρχικό στάδιο του πρωτοπαθούς όγκου
- Ο χρόνος ανίχνευσης των μεταστάσεων
- Ο τύπος της ηπατεκτομής
- Οι προεγχειρητικές τιμές CEA
- Το ιστορικό προηγούμενης ηπατεκτομής
Όρια εκτομής
Θετικά όρια εκτομής (R1 ή R2 εκτομή), έχει αποδειχθεί από σειρά μελετών, ότι συνιστούν ένα πολύ κακό προγνωστικό παράγοντα. Η R0 εκτομή (ιστολογικά αρνητικά όρια εκτομής) μειώνει την τοπική υποτροπή και βελτιώνει τη διάμεση επιβίωση σχεδόν στο διπλάσιο (24 έναντι 46 μηνών). Εκτιμώντας ότι η επίτευξη ενός αρνητικού ορίου εκτομής είναι σημαντική, η έκταση του όμως είναι αμφισβητούμενη. Διάφορες προηγούμενες σειρές
συνιστούν το όριο αυτό εκτομής να είναι στο 1 cm, υποδεικνύουν δε ότι η μη προσδοκώμενη επίτευξή του αποτελεί σχετική αντένδειξη ηπατεκτομής.
Άλλοι συγγραφείς σε πιο πρόσφατες μελέτες υποδεικνύουν, ότι το πραγματικό πλάτος του χειρουργικού ορίου εκτομής δεν έχει καμία επίδραση στην επιβίωση, εφ’ όσον το όριο αυτό είναι ιστολογικά αρνητικό (R0).
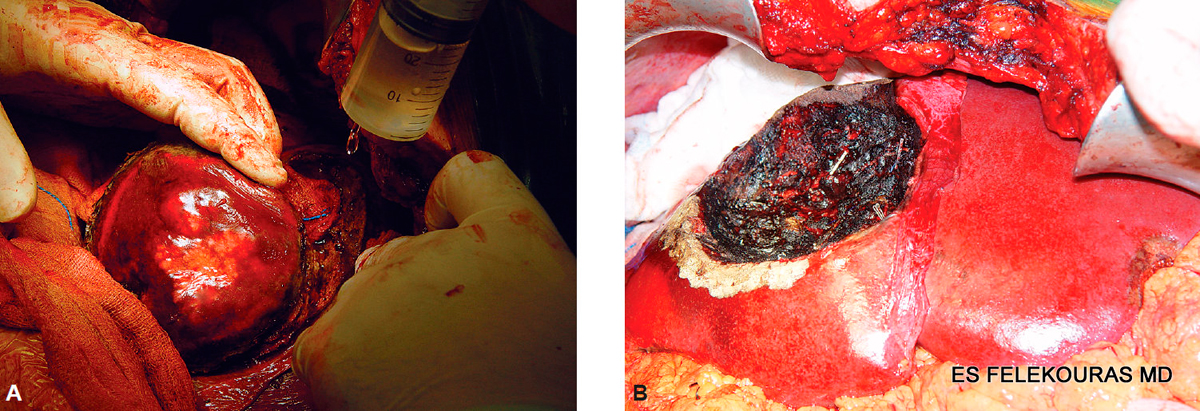
Συνεπώς, πρέπει να συνεχίσουμε – για να μην μεταβούμε στο άλλο άκρο – να προγραμματίζουμε την ηπατεκτομή για ΜΝΗ από ορθοκολικό καρκίνο, διατηρώντας ένα «όριο ασφάλειας» και να αποφεύγουμε αν μπορούμε την εκτομή επάνω στον όγκο, που είναι το «ελάχιστο όριο». Εντούτοις, βασισμένοι στο σύνολο των στοιχείων, ένα χειρουργικό όριο τουλάχιστον 1 mm δεν θέτει τον ασθενή σε κίνδυνο υποτροπής ή σε χειρότερη πρόγνωση. Επομένως, το προβλεφθέν όριο εκτομής <1 cm δεν πρέπει να χρησιμοποιείται ως κριτήριο αποκλεισμού εκτέλεσης της ηπατεκτομής (εικόνα 9 και 10).
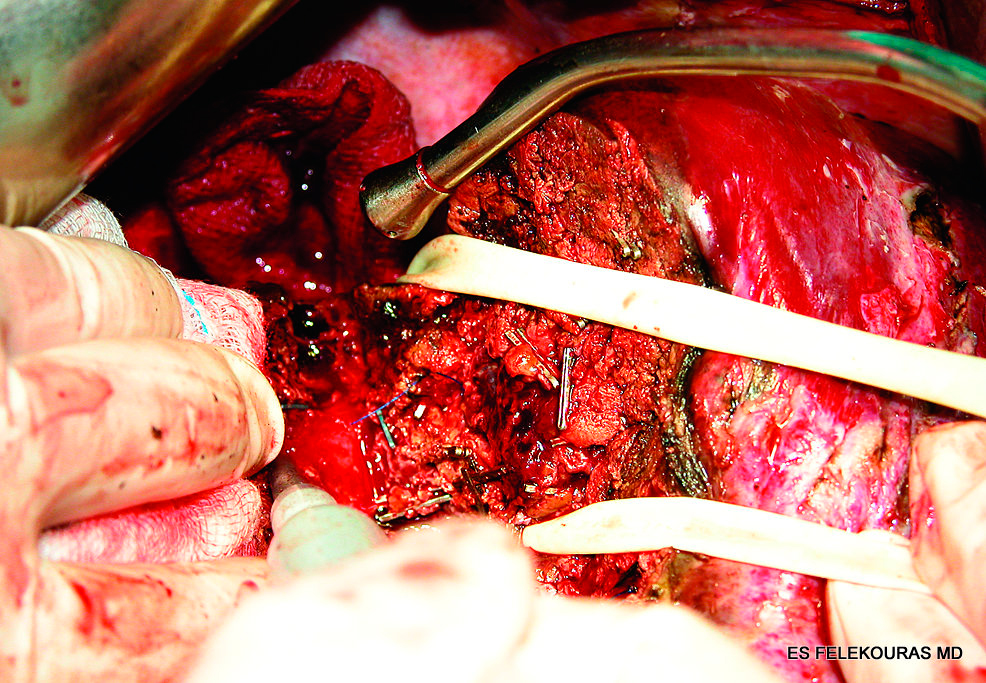
Εικόνα 9: Όρια εκτομής σε RFA (υποβοηθούμενη ηπατεκτομή) για ΜΝΗ. Χαρακτηριστική είναι η απουσία μακροσκοπικώς εμφανούς νόσου στην επιφάνεια διατομής, η οποία επιζητείται στα πλαίσια επιδίωξης μιας R0 εκτομής.
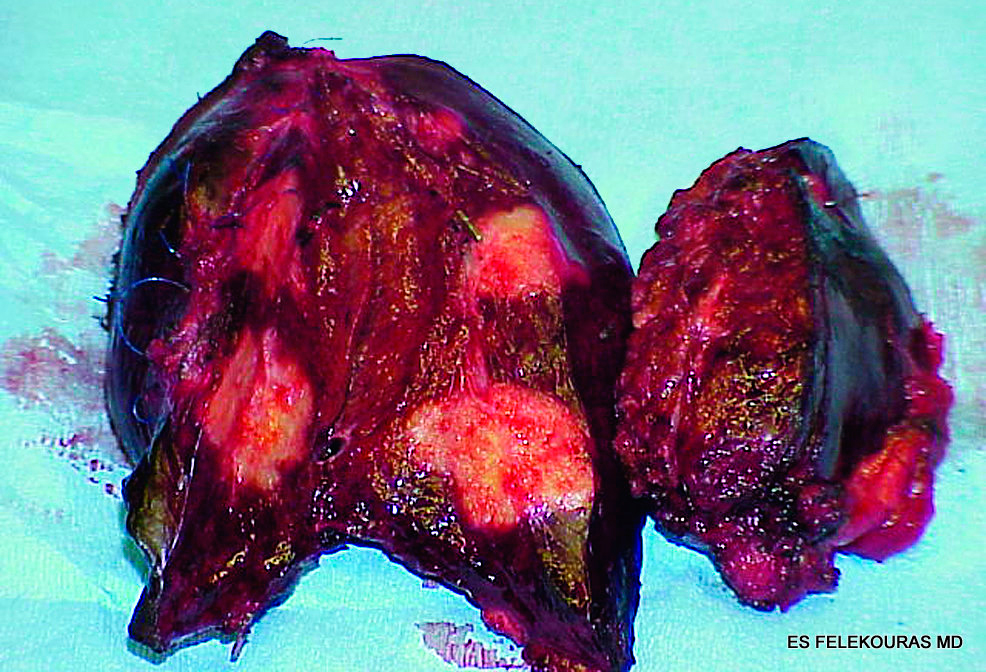
Εικόνα 10: Παρασκεύασμα ηπατεκτομής για ΜΝΗ από ορθοκολικό καρκίνο. Σε εγκάρσια διατομή διακρίνονται οι μεταστατικές εστίες, καθώς και η μακροσκοπική εξασφάλιση ορίων εκτομής >1 εκατοστού.
Ηπατεκτομή σε έδαφος λεμφαδένων στην πύλη του ήπατος.
Όσον αφορά στις μεταστάσεις στους λεμφαδένες της πύλης του ήπατος, θα πρέπει να αναφερθούν ορισμένα στοιχεία που πιθανώς να αποσαφηνίσουν την αξία της ηπατικής χειρουργικής, στην ειδική αυτή ομάδα ασθενών με ΜΝΗ. Οι μεταστάσεις στους λεμφαδένες της πύλης του ήπατος αναγνωρίζονται ως σημαντικός προγνωστικός παράγοντας, μιας και θεωρούνται «μεταστάσεις των μεταστάσεων» και συνδέονται με
πτωχή έκβαση.
Άλλες μελέτες, εντούτοις, έχουν δείξει ότι και στους ασθενείς αυτούς μπορούμε να επιτύχουμε μακρά επιβίωση μετά από ηπατεκτομή, η οποία μπορεί να φθάσει και στο 41,7%. Με βάση τα στοιχεία αυτά η παρουσία μεταστατικών λεμφαδένων στην πύλη του ήπατος, ενώ συνδέεται βεβαίως με χειρότερη έκβαση, δεν πρέπει να αποτελέσει κριτήριο αποκλεισμού της ηπατεκτομής. Μερικοί συγγραφείς συνιστούν το λεμφαδενικό καθαρισμό
του ηπατοδωδεκαδακτυλικού συνδέσμου, ως απαραίτητο τμήμα κάθε ηπατεκτομής. Η προσθήκη όμως της διαδικασίας αυτής ως ρουτίνας στην ηπατεκτομή για ΜΝΗ από ορθοκολικό καρκίνο παραμένει αμφισβητούμενη.
Ηπατεκτομή σε έδαφος περιτοναϊκών μεταστάσεων.
Το περιτόναιο συνιστά την αρχική εστία υποτροπής μετά από θεραπευτική κολεκτομή στο 10-20%, συμμετέχει δε στο 40-70% των περιπτώσεων συμμετέχει δε στο 40-70% των περιπτώσεων που παρουσιάζονται με προχωρημένη νόσο και οι οποίοι εμφανίζουν κακή πρόγνωση (διάμεση επιβίωση 5-9 μήνες).
Για την πλειονότητα των χειρουργών η διάχυτη καρκινωμάτωση είναι ανάλογη των απομακρυσμένων μεταστάσεων. Ο Sugarbaker όμως πρώτος πρότεινε ότι η κατάσταση αυτή συνιστά περιοχική νόσο και πρότεινε την αντιμετώπισή της με κυτταρομειωτική θεραπεία (cytoreductive surgery, CS) σε συνδυασμό με ενδοπεριτοναϊκή υπερθερμική χημειοθεραπεία (hyperthermic intraperitoneal chemotherapy, HIPEC), για την εξάλειψη της
μικροσκοπικής υπολειπόμενης νόσου. Ο Elias επίσης δημοσίευσε μελέτη ασθενών, που η ηπατεκτομή σε συνδυασμό με λεμφαδενικό καθαρισμό της πύλης του ήπατος, χημειοθεραπεία και CS-HIPEC οδήγησε σε διάμεση επιβίωση 38 μηνών, 5ετή επιβίωση 32%, καθώς και με θνητότητα και νοσηρότητα 3% και 18%, αντίστοιχα. Αν και ασθενείς με εξωηπατική νόσο ενεφάνισαν μικρότερη 5ετή επιβίωση (28%), αυτή ήταν καλύτερη από την επιβίωση της απλής χημειοθεραπείας (διάμεση επιβίωση 22-24 μήνες). Συνεπώς, επεμβάσεις όπως και αυτές, θα μπορούσαν να συμπεριληφθούν στο οπλοστάσιό μας και στην καθημέρα πράξη, αν και αυτό δεν είναι αποδεικτικό τόσο από οικονομικής άποψης, όσο και λόγω έλλειψης πραγματικής βάσης δεδομένων.
Ηπατεκτομή επί ηπατικών και πνευμονικών μεταστάσεων.
Η θεραπευτική κολεκτομή για ορθοκολικό καρκίνο (στάδια Α, Β, C κατά Dukes) δεν οδηγεί πάντα στην ίαση, άνω δε των 40% των ασθενών υποτροπιάζουν. Οι πιο συχνές εστίες υποτροπής είναι το ήπαρ (33%) και οι πνεύμονες. Συνεπώς το ενδιαφέρον δεν εστιάζεται μόνο στη ΜΝΗ από ορθοκολικό καρκίνο, αλλά και στη σύγχρονη ή μετάχρονη θεραπεία της ΜΝΠ (μεταστατική νόσο των πνευμόνων) από αυτόν τον καρκίνο (εικόνα 11).
Εικόνα 11: Μονήρης μεταστατική νόσος του πνεύμονα στο δεξιό μέσο λοβό από ορθοκολικό καρκίνο.
Κολεκτομή και σύγχρονη έναντι μετάχρονης ηπατεκτομής
Αν η ΜΝΗ είναι σύγχρονη με τον ορθοκολικό καρκίνο και ειδικά όταν ανευρεθεί κατά τη διάρκεια της χειρουργικής επέμβασης για την κολεκτομή, τότε όλη η περιτοναϊκή κοιλότητα πρέπει να εξεταστεί πολύ προσεκτικά για άλλες μεταστάσεις. Αν δεν υπάρχει αλλού νόσος και η βλάβη στο ήπαρ μπορεί να εξαιρεθεί με αρνητικά όρια εκτομής και χωρίς ιδιαίτερη νοσηρότητα και θνητότητα, τότε πρέπει με μια μικρή, μη ανατομική εκτομή αυτή να αφαιρεθεί. Αν μια μεγαλύτερη ηπατεκτομή είναι απαραίτητη, η δε επιλογή της δεν είχε συζητηθεί με τον ασθενή προεγχειρητικά, τότε οι περισσότεροι χειρουργοί θα περιορίζονταν μόνο στην εκτέλεση κολεκτομής. Στην περίπτωση αυτή, ο ασθενής προετοιμάζεται για ένα διάστημα 3-6 μηνών με χημειοθεραπεία και κατόπιν οδηγείται εκ νέου στο χειρουργείο για ηπατεκτομή.
Όταν η ΜΝΗ ανευρεθεί προ της κολεκτομής, τότε πρέπει να εξεταστεί η περίπτωση της σύγχρονης αντιμετώπισης (εικόνα 12). Οι περισσότεροι χειρουργοί προχωρούν όμως στην κολεκτομή και ακολουθούν την ανωτέρω αναφερθείσα προσέγγιση, μιας και η καθυστέρηση εκτέλεσης ειδικά μεγάλης ηπατεκτομής παρέχει αρκετά πλεονεκτήματα. Μια τέτοια μελέτη διαπίστωσε, ότι ασθενείς που υπεβλήθησαν σε καθυστερημένη ηπατεκτομή
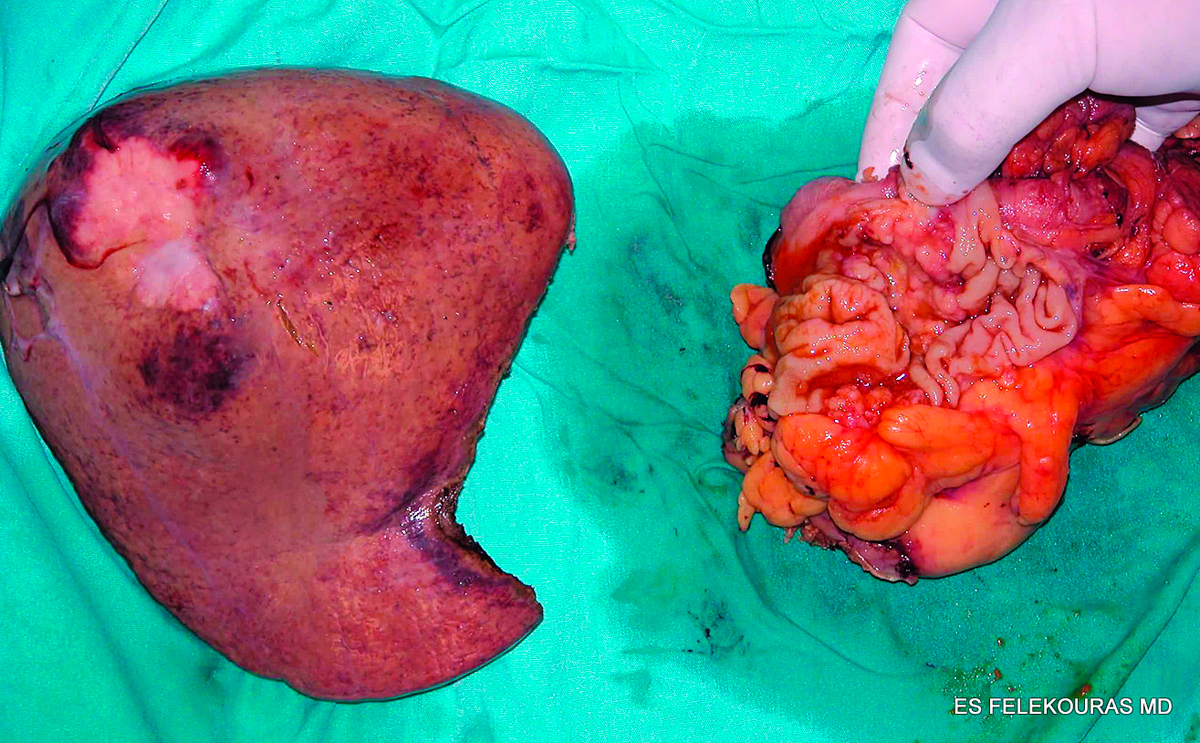
και τους χορηγήθηκε προηγουμένως χημειοθεραπεία, είχαν καλύτερη έκβαση από εκείνους που χειρουργήθηκαν με σύγχρονη ηπατεκτομή για τη θεραπεία της ΜΝΗ από ορθοκολικό καρκίνο.
Εικόνα 12: Εγχειρητικό παρασκεύασμα ασθενούς που υπεβλήθη σε αριστερή ημικολεκτομή και σύγχρονη τμηματεκτομή και σφηνοειδή εκτομή στα πλαίσια σχεδιασμένης επέμβασης για ΜΝΗ.
Τα πιθανά μειονεκτήματα της σύγχρονης ηπατεκτομής περιλαμβάνουν τη διεγχειρητική επιμόλυνση της διαταμείσας επιφάνειας του ήπατος, με συνέπεια το σχηματισμό αποστήματος, την πιθανή διάσπαση της αναστόμωσης του παχέος εντέρου λόγω της κακής μετεγχειρητικής λειτουργίας του ήπατος, και τη δυνατότητα/πιθανότητα για υψηλότερα ποσοστά υποτροπής, λόγω πιθανής διασποράς του όγκου. Γενικά, η σύγχρονη ηπατεκτομή
δεν συνιστάται σε ηλικιωμένους ασθενείς (>70 έτη), όταν ένα μεγάλο τμήμα (sector) πρόκειται να αφαιρεθεί και ο όγκος του παχέος εντέρου δεν είναι καλά διαφοροποιημένος ή πρόκειται περί ενός βλεννώδους αδενοκαρκινώματος. Σήμερα όπως μεγάλες σύγχρονες επεμβάσεις (κολεκτομή και ηπατεκτομή) κάνουμε σε ασθενείς μετά από λεπτομερή προεγχειρητικό έλεγχο και επιλογή ασθενών.
Σήμερα πιστεύεται, ότι αρκετοί ασθενείς με συμπτωματικούς πρωτοπαθείς όγκους του παχέος εντέρου και με εξαιρέσιμες ηπατικές μεταστάσεις, θα μπορούσαν να εξαιρεθούν συγχρόνως και εν συνεχεία να ακολουθήσει χημειοθεραπεία. Οι ασυμπτωματικοί, υψηλού όμως κινδύνου ασθενείς, πρέπει πρώτα να λάβουν neoadjuvant συστηματική χημειοθεραπεία, υπάρχουν δε και νεότερα δεδομένα που μας κάνουν να πιστεύουμε ότι όλοι οι ασθενείς με εξαιρέσιμη ηπατική νόσο θα πρέπει να υποβληθούν πρώτα σε χημειοθεραπεία. Αν η προεγχειρητική αξιολόγηση δείξει ότι ένας ασθενής εμφανίζει
βιολογικά και τεχνικά εξαιρέσιμες μεταστάσεις του ήπατος, πρέπει στη συνέχεια να αξιολογηθούν προσεκτικά τα συμπαραμαρτούντα νοσήματα, όσον αφορά τον κίνδυνο της χειρουργικής επέμβασης. Η προεγχειρητική καρδιοπνευμονική λειτουργία οφείλει να αξιολογηθεί λεπτομερώς. Η χρονολογική ηλικία δεν είναι τόσο σημαντική όσο η φυσιολογική ηλικία, η οποία αντικατοπτρίζει και τη γενική κατάσταση του οργανισμού, ενώ παίζει ρόλο.
Άλλοι θεραπευτικοί και χειρουργικοί χειρισμοί που προάγουν τη βελτίωση της εξαιρεσιμότητας
Προεγχειρητική συστηματική χημειοθεραπεία
Μια προσέγγιση όσον αφορά τη βελτίωση της εξαιρεσιμότητας είναι η υποσταδιοποίηση (downstaging), αλλά κυρίως η ελάττωση του μεγέθους (downsizing) μη χειρουργήσιμων μεταστάσεων με συστηματική χημειοθεραπεία (εικόνα 13). Ένα ποσοστό περί το 10-15% των μη χειρουργήσιμων ασθενών μπορεί να καταστούν χειρουργήσιμοι, ενώ το 93% των ασθενών αυτών είναι δυνατόν να υποβληθεί σε θεραπευτική εκτομή με πενταετή και
δεκαετή επιβίωση 33% και 23%, αντίστοιχα. Η πρόοδος του όγκου κατά τη διάρκεια της συστηματικής θεραπείας είναι μια σχετική αντένδειξη για ηπατεκτομή. Η ηπατεκτομή πρέπει να εκτελεστεί μόλις η ασθένεια καταστεί εξαιρέσιμη. Οι τρέχουσες μελέτες χημειοθεραπείας χρησιμοποιούν νέα βιολογικά και συστηματικά φάρμακα για να αυξήσουν τον αριθμό των ασθενών, που θα μετατεθούν στην ομάδα των υποψηφίων για ηπατεκτομή.
Εικόνα 13: Υπολογιστική αξονική τομογραφία (CΤ) απεικόνιση ΜΝΗ (αρκετές και στους δυο λοβούς), σε ασθενή που υπεβλήθει σε συνδυασμό μεθόδων θεραπείας (προ- εγχειρητική συστηματική χημειοθεραπεία (the liver first approach), ηπατεκτομή 2 σταδίων και ΗΑΙ και τελικά κατέστη κατάλληλος υποψήφια για χειρουργική θεραπεία (κάτω) και στην τελευταία εικόνα η τελική ΑΤ του ασθενούς μετά την δεξιά ηπατεκτομή (διακρίνεται ο καθετήρας της ηπατικής αρτηρίας που χρησιμοποιήθηκε για ΗΑΙ). Στην τελική εικόνα η ΑΤ της ασθενούς 8 χρόνια μετά την ολοκλήρωση της θεραπείας της
Διαδερμικός διηπατικός ομόπλευρος εμβολισμός της πυλαίας φλέβας (PVE), απολίνωση πυλαίας φλέβας
Είναι γενικά αποδεκτό ότι περίπου το 25% του συνολικού όγκου του ήπατος πρέπει να διατηρηθεί ως φυσιολογικό ήπαρ μετά από ηπατεκτομή, για να ελαχιστοποιηθεί ο κίνδυνος ηπατικής ανεπάρκειας, που αποτελεί την κύρια πηγή νοσηρότητας και θνητότητας μετά από ηπατεκτομή. Για ασθενείς με κίρρωση ή εκείνους που υποβάλλονται σε συστηματική χημειοθεραπεία, σύμφωνα με πολλούς συγγραφείς, το ποσοστό 40% πρέπει να είναι το
ασφαλές κατώτατο όριο. Οι Makuuchi και συν., πρώτοι δημοσίευσαν (σε ηπατεκτομές για χολαγγειοκαρκίνωμα) ότι η ηπατική αυτή ανεπάρκεια δεν συμβαίνει σε ασθενείς που είχαν προεγχειρητικά υποβληθεί σε εμβολισμό της πυλαίας φλέβας του λοβού που επρόκειτο να αφαιρεθεί, με αποτέλεσμα ο PVE να εισέλθει στο οπλοστάσιο μας το 1990. Ο PVE οδηγεί στη συρρίκνωση του ήπατος που πρόκειται να αφαιρεθεί και του οποίου η πυλαία φλέβα εμβολίζεται (ομόπλευρα) και διεγείρει την αύξηση του ιστού του τμήματος που θα παραμείνει (το μελλοντικό υπόλοιπο ήπαρ, Future Liver Remnant, FLR) (εικόνα 14 και 15). Η διαδικασία αυτή προάγεται μέσω εισαγωγής της απόπτωσης των ηπατοκυττάρων, που στερούνται της πυλαίας κυκλοφορίας και όχι της νέκρωσης, καθώς και με αναγέννηση των υγιών ηπατοκυττάρων, μια διαδικασία που αρχίζει μέσα σε μία ημέρα μετά τον εμβολισμό και φθάνει στο μέγιστο σε 12-14 ημέρες, ολοκληρώνεται δε σε 4 περίπου εβδομάδες (μελέτες σε πειραματόζωα) με αύξηση του όγκου του FLR από 7% έως και 40%
.
Εικόνα 14: Ακτινοσκοπική απεικόνιση διαδερμικού καθετηριασμού του στελέχους της δεξιάς πυλαίας φλέβας με σκιαγράφηση αυτής και έγχυση υλικού αποκλεισμού της αιμάτωσης.
Εικόνα 15: Με MRI και ΑΤ απεικόνιση του πυλαίου δικτύου μετά από επιτυχή διαδερμικό εμβολισμό του δεξιού κλάδου της ΠΦ. Είναι χαρακτηριστική η απουσία σκιαγράφηση της πυλαίας αιμάτωσης του δεξιού λοβού του ήπατος, καθώς και η αρχόμενη υπερτροφία του ετέρου (αριστερού λοβού).
Είναι γενικά αποδεκτό ότι περίπου το 25% του συνολικού όγκου του ήπατος πρέπει να διατηρηθεί ως φυσιολογικό ήπαρ μετά από ηπατεκτομή, για να ελαχιστοποιηθεί ο κίνδυνος ηπατικής ανεπάρκειας, που αποτελεί την κύρια πηγή νοσηρότητας και θνητότητας μετά από ηπατεκτομή. Για ασθενείς με κίρρωση ή εκείνους που υποβάλλονται σε συστηματική χημειοθεραπεία, σύμφωνα με πολλούς συγγραφείς, το ποσοστό 40% πρέπει να είναι το
ασφαλές κατώτατο όριο. Οι Makuuchi και συν., πρώτοι δημοσίευσαν (σε ηπατεκτομές για χολαγγειοκαρκίνωμα) ότι η ηπατική αυτή ανεπάρκεια δεν συμβαίνει σε ασθενείς που είχαν προεγχειρητικά υποβληθεί σε εμβολισμό της πυλαίας φλέβας του λοβού που επρόκειτο να αφαιρεθεί, με αποτέλεσμα ο PVE να εισέλθει στο οπλοστάσιο μας το 1990. Ο PVE οδηγεί στη συρρίκνωση του ήπατος που πρόκειται να αφαιρεθεί και του οποίου η πυλαία φλέβα εμβολίζεται (ομόπλευρα) και διεγείρει την αύξηση του ιστού του τμήματος που θα παραμείνει (το μελλοντικό υπόλοιπο ήπαρ, Future Liver Remnant, FLR) (εικόνα 14 και 15). Η διαδικασία αυτή προάγεται μέσω εισαγωγής της απόπτωσης των ηπατοκυττάρων, που στερούνται της πυλαίας κυκλοφορίας και όχι της νέκρωσης, καθώς και με αναγέννηση των υγιών ηπατοκυττάρων, μια διαδικασία που αρχίζει μέσα σε μία ημέρα μετά τον εμβολισμό και φθάνει στο μέγιστο σε 12-14 ημέρες, ολοκληρώνεται δε σε 4 περίπου εβδομάδες (μελέτες σε πειραματόζωα) με αύξηση του όγκου του FLR από 7% έως και 40%.
Ηπατεκτομή δύο σταδίων (Staged resection)
Ένας αριθμός ασθενών με πολλαπλές μεταστάσεις δεν είναι υποψήφιοι για μια πλήρη εκτομή των μεταστάσεών τους με ηπατεκτομή, ακόμα και μετά από PVE ή συρρίκνωση από χημειοθεραπεία. Μια διαδοχική ή η δύο σταδίων ηπατεκτομή μπορεί επομένως να είναι απαραίτητη για να επιτευχθεί η πλήρης χειρουργική εξάλειψη όλων των γνωστών μεταστάσεων. Κατά τη διάρκεια της πρώτης επέμβασης, ο μεγαλύτερος πιθανός αριθμός
μεταστάσεων εξαιρείται. Μετεγχειρητικά, το υπόλοιπο ήπαρ αναγεννάται, η δε λειτουργική του ικανότητα βελτιώνεται. Η ανάπτυξη των μεταστάσεων αντιμετωπίζεται με συστηματική χημειοθεραπεία κατά τη διάρκεια της περιόδου αναμονής. Μια δεύτερη ηπατεκτομή εκτελείται μετά πάροδο μερικών εβδομάδων ή μηνών. Η μέθοδος μπορεί να συνδυασθεί με ή χωρίς PVE ή RFA.
Το πλεονέκτημα της μεθόδου κατά το πρώτο στάδιο είναι η συντήρηση ενός μέγιστου ποσού ηπατικού παρεγχύματος, το όποιο θα υπερτραφεί και το οποίο καθίσταται τελικά το λειτουργικό υπόλοιπο του ήπατος μετά και από τη δεύτερη ηπατεκτομή. Η δύο σταδίων ηπατεκτομή πρέπει να εκτελείται μόνον με θεραπευτική πρόθεση, η δε εφαρμογή της στρατηγικής αυτής πρέπει να εξετάζεται πολύ προσεκτικά, ώστε να αποφεύγεται η
μετεγχειρητική ηπατική ανεπάρκεια. Η 3ετής επιβίωση μετά από μια τέτοια ηπατεκτομή μπορεί να φθάσει στο 35-39%.
ALPPS
H ALPPS είναι η πιο πρόσφατη τροποποίηση από τις τεχνικές που αναπτύχθηκαν για ηπατεκτομές δύο σταδίων που επιτρέπουν εκτομή των όγκων του ήπατος σε δύο βήματα, κάνοντας χρήση της αναγεννητικής του ικανότητας του ανθρώπινου ήπατος. Η ALPPS μας είναι πρακτικά ίδια με την ηπατεκτομή 2 σταδίων αλλά δεν γίνεται απλά απολίνωση της δεξιάς κυρίως αλλά και της αριστερής ΠΦ αλλά και διατομή του ηπατικού παρεγχύματος κατά την γραμμή ισχαιμίας χωρίς όμως να διακοπεί η αντίστοιχη ηπατική φλέβα. Έτσι επιτρέπει να αφαιρέσουμε ένα εκτεταμένο μέρος του ήπατος σε δύο βήματα (2 επεμβάσεις). Μετά από μια περίοδο αναμονής για 1-2 εβδομάδες το δεύτερο βήμα γίνεται και εκτέμνεται το αντίστοιχο τμήμα του ήπατος.
Η νέα στρατηγική προσφέρει δύο πλεονεκτήματα: πρώτα κομψά αντιμετωπίζεται η πιο μεγάλη επιπλοκή μετά από μεγάλες ηπατεκτομές, δηλαδή η “μετεγχειρητική ηπατική ανεπάρκεια”. Το πάσχον ημιήπαρ, παραμένει στη θέση του, και ενεργεί ως ένα βοηθητικό ήπαρ ικανό να βοηθήσει το μελλοντικό εναπομείναν ήπαρ για την πρώτη και κρίσιμη εβδομάδα μετά την εκτομή. Δεύτερον, αυτή η νέα λειτουργία προκαλεί ένα ποσό της
υπερτροφίας που είναι καλύτερο από άλλες τεχνικές όπως ο PVE η PVL προκαλώντας μια αύξηση 74% του όγκου του εναπομείναντος ήπατος σε έναν μέσο όρο 9 ημέρες μετεγχειρητικά, όμως έχει το μειονέκτημα ότι ο ασθενής υποβάλλεται σε δυο επεμβάσεις μέσα σε σύντομο χρονικό διάστημα με ότι αυτό σημαίνει (εικόνα 16).
Εικόνα 16: Η ηπατεκτομή 2 σταδίων κατά ALPPS (courtesy Dr A Papalambros, Hamburg. Germany)
Σύνοψη αποτελεσμάτων ηπατεκτομής
Η ηπατεκτομή εκτελείται συνήθως κατά τον παραδοσιακό τρόπο (ανοικτή χειρουργική επέμβαση) με αρκετά μεγάλες τομές. Όλο όμως και περισσότερες αναφορές υπεισέρχονται στη βιβλιογραφία για μείζονες και ελάσσονες λαπαροσκοπικές ηπατεκτομές με καλά αποτελέσματα.
Η θνητότητα μετά από ηπατεκτομή για ΜΝΗ από ορθοκολικό καρκίνο πρέπει να είναι μικρότερη από 5% και η νοσηρότητα επίσης σχετικά μικρή (8-24%). Το ογκολογικό αποτέλεσμα της ηπατεκτομής εξαρτάται από πολλούς παράγοντες, μερικοί εκ των οποίων είναι:
- τα όρια εκτομής (R0 ή R1 ), ενώ συγκεκριμένα ένα αρνητικό όριο μεγαλύτερο του 1 mm είναι σημαντικό. Τα αποτελέσματα θεωρούνται καλύτερα όταν τα όρια είναι μεταξύ 1 και 10 mm συγκρινόμενα με τα αντίστοιχα θετικά όρια, ενώ δεν υπάρχει καμία διαφορά μεταξύ ορίων 1-4 mm έναντι 5-9 mm, και
- όταν σε μια ηπατεκτομή υφίστανται αρνητικά όρια εκτομής, τότε η απώτερη επιβίωση εξαρτάται από πολλούς άλλους παράγοντες.
Η νοσηρότητα και η θνητότητα μετά από ηπατεκτομή είναι σημαντικές, παρόλο που σήμερα οι επεμβάσεις επί του οργάνου αυτού πραγματοποιούνται με ασφάλεια και χωρίς μείζονα προβλήματα. Οι μετεγχειρητικές επιπλοκές προέρχονται συνήθως από το καρδιοαναπνευστικό σύστημα (κυρίως πνευμονία, 5-22%), είναι δε η πλευριτική συλλογή (5-10%), οι τοπικές σηπτικές επιπλοκές, όπως τα υφηπατικά ή υποδιαφραγματικά αποστήματα (2-10%), καθώς και η μετεγχειρητική αιμορραγία, που είναι αρκετά συχνή σε ορισμένες ομάδες ασθενών. Ειδικές επιπλοκές της ηπατεκτομής αποτελούν κυρίως η χολόρροια με χοληφόρο συρίγγιο (4%), η ηπατική ανεπάρκεια (3-8%) και η πνευμονική
εμβολή (1%). Η καταγραφή των επιπλοκών στην πορεία του χρόνου καθώς και η ανάπτυξη μηχανισμών και αλγορίθμων πρόληψης και αντιμετώπισης, επέφεραν σημαντικά αποτελέσματα στο επίπεδο της στατιστικής βελτίωσης των ποσοστών νοσηρότητας, και όχι μόνον. Έτσι, με την πάροδο των ετών η θνητότητα μετά από ηπατεκτομή έπεσε σταδιακά από το 20% στη δεκαετία του ’80 στο 1% περίπου των τελευταίων ετών.
Σήμερα, όλο και περισσότερες μελέτες αναφέρουν 5ετείς επιβιώσεις πλησίον του 40% για τη θεραπεία της ΜΝΠ, χωρίς η επιβίωση αυτή να επηρεάζεται από την παρουσία ή όχι στο παρελθόν ηπατεκτομής για ΜΝΗ. Τα κύρια προγνωστικά σημεία των μελετών αυτών είναι η
R0 εκτομή της ΜΝΗ, διάστημα ελεύθερο νόσου >36 μηνών και οι μονήρεις μεταστάσεις. Ακόμα και στους ασθενείς αυτούς με κακά προγνωστικά σημεία η επιβίωση ευρέθη να είναι καλύτερη μετά από εκτομή των μεταστάσεων συγκριτικά με αυτούς με μόνη χημειοθεραπεία. Η 5ετής επιβίωση ασθενών με εκτομή μέχρι 3 μεταστάσεων αναφέρθηκε 50%, αυτή δε περισσότερων από 4 μεταστάσεων οδήγησε σε 100% υποτροπή μέσα σε 16
μήνες. Η δεκαετής επιβίωση μετά από χειρουργική θεραπεία ΜΝΗ (μονήρων ή πολλαπλών) από ορθοκολικό καρκίνο είναι περίπου 31%. Έτσι, η υποτροπή στον πνεύμονα είναι συνήθης, αλλά η νέα εκτομή είναι ενδεδειγμένη, μιας και η 5ετής επιβίωση ευρέθη περίπου 30%, ενώ στους μη χειρουργήσιμους όγκους ίσως το RFA του πνεύμονα να αποτελεί μια λύση, ειδικά δε όταν οι εστίες είναι μικρότερες από 3 cm.
Φυσικά η υποτροπή μετά από ηπατεκτομή είναι συνήθης (65%). Περίπου το 40% από τους ασθενείς υποτροπιάζουν μόνο στο ήπαρ, μπορεί δε να υποβληθούν σε 2η και πολλές φορές και 3η ηπατεκτομή με σχετικά ικανοποιητική 5ετή επιβίωση γύρω στο 26% και διάμεση 30 μηνών (εικόνα 18). Πρέπει όμως να τονισθεί, ότι στις περιπτώσεις αυτές το ήπαρ είναι πιο εύθρυπτο και με πολλές συμφύσεις, η δε επέμβαση καθίσταται δυσκολότερη.
Άλλες επεμβάσεις πέραν της μερικής ηπατεκτομής, όπως π.χ. η μεταμόσχευση ήπατος (ΜΗ), δεν αποτελούν θεραπευτική επιλογή για τη νόσο αυτή, μιας και τα αποτελέσματα της δεκαετίας του ’80 και των αρχών του ’90 ήταν απογοητευτικά. Σήμερα, όμως, ειδικά πρωτόκολλα ευρίσκονται εν εξελίξει σε πολλά κέντρα της Ευρώπης και των ΗΠΑ, θα μπορούσε δε να λεχθεί ότι και ο ρόλος της μεταμόσχευση ήπατος (ΜΗ) ειδικά από ζώντα δότη υπό κάποιες πολύ αυστηρές προϋποθέσεις ευρίσκεται υπό εξέταση.
Εικόνα 17: Αποτελέσματα ηπατεκτομής για ΜΝΗ-ΚΟ
Άλλες θεραπευτικές επιλογές πέραν της χειρουργικής
Σε ανεγχείρητες περιπτώσεις αλλά και ως μετεγχειρητική συμπληρωματική θεραπεία, η ακόμα κατά την διάρκεια μιας ηπατεκτομής, χρησιμοποιούνται διάφορες μέθοδοι, όπως η χημειοθεραπεία και η θερμική καταστροφή του όγκου.
Συστηματική χημειοθεραπεία
Στους ασθενείς με ανεγχείρητους όγκους με σύγχρονη ή μετάχρονη ΜΝΗ πρέπει να προχωρούμε άμεσα σε χημειοθεραπεία με τη σκέψη ότι η θεραπεία αυτή είναι neoadjuvant μορφή σχήματος, μιας και όπως ελέχθει, η πιθανότητα να ανταποκριθεί ένας τέτοιος ασθενής είναι αρκετά υψηλή, με μέση επιβίωση να ξεπερνά τους 24 μήνες. Μετά από κάθε 6 πλήρεις κύκλους θεραπείας ο ασθενής επανελέγχεται με ΑΤ κοιλίας και θώρακα, αν δε κριθεί ότι η νόσος είναι χειρουργήσιμη, ο ασθενής υποβάλλεται σε χειρουργική αντιμετώπισή της. Στις περισσότερες σειρές ένα 15%-30% των ασθενών που
είχαν αρχικά εμφανίσει ανεγχείρητο ΜΝΗ, υπεβλήθησαν σε θεραπευτική ηπατεκτομή, ενώ σε μια μελέτη η 5ετής επιβίωση των ασθενών αυτών έφθασε στο 40%. Θα έπρεπε κατά μερικούς, η neoadjuvant αυτή χημειοθεραπεία να ονομάζεται θεραπεία μετατροπής – «Conversion therapy» – αφού προσπαθεί να μετατρέψει τη νόσο από ανεγχείρητη σε χειρουργήσιμη. Φυσικά, στην προσπάθεια αυτή δεν χρησιμοποιείται μόνον η ημειοθεραπεία, αλλά συγχρόνως και άλλες τεχνικές όπως έχει ήδη προαναφερθεί, αυτές δε είναι κυρίως ο PVE, το RFA και η ηπατεκτομή 2 σταδίων.
Σήμερα πιστεύεται, ότι το καλύτερο για όλους τους ασθενείς που υποβάλλονται σε ηπατεκτομή για ΜΝΗ από ορθοκολικό καρκίνο είναι να τους χορηγηθεί πρώτα χημειοθεραπεία, αφού και τα αποτελέσματα είναι καλυτέρα και βελτιωμένα κατά 25% τουλάχιστον.
Η προεγχειρητική συστηματική θεραπεία στα πλαίσια της neoadjuvant μεθόδου χορήγησης είναι σημαντική και για μια μικρή ομάδα ασθενών που είναι επικίνδυνο να υποβληθούν άμεσα σε σύγχρονη εκτομή του όγκου και ηπατεκτομή, αλλά και συγχρόνως η κατάσταση του ήπατος από την έκταση του όγκου, δεν τους επιτρέπει την ασφαλή επέμβαση, λόγω κυρίως μετεγχειρητικής ηπατικής ανεπάρκειας και ικτέρου. Τέτοιοι ασθενείς πρέπει άμεσα να υποβληθούν σε θεραπεία για τη ΜΝΗ και όχι για την πρωτοπαθή εστία, αφού δε διαφύγουν τον κίνδυνο ανάπτυξης ηπατικής ανεπάρκειας, να υποβληθούν εν συνέχεια σε κολεκτομή και ηπατεκτομή ή ακόμη και σε επέμβαση 2 σταδίων. Σε ασθενείς που η ηπατική ανεπάρκεια και ο ίκτερος αποτελούν τα πρώτα συμπτώματα της νόσου, θα πρέπει να εξετασθεί η πιθανότητα διενέργειας παροχετευτικών επεμβάσεων των χοληφόρων (κυρίως PTC), αν διαπιστωθεί ότι ο ίκτερος οφείλεται σε απόφραξη των εξωηπατικών χοληφόρων, με σκοπό να δοθεί και στους ασθενείς αυτούς η δυνατότητα να υποβληθούν σε χημειοθεραπεία και ίσως αν ανταποκριθούν και σε χειρουργική αποκατάσταση της νόσου τους. Εδώ πρέπει να σημειωθεί, ότι η χορήγηση χημειοθεραπείας σε ασθενείς με ίκτερο (χολερυθρίνη >3 mg/dl) είναι τοξική και δεν επιτρέπεται.
Όσον αφορά όμως σε ασθενείς που υποβάλλονται σε συστηματική ή neoadjuvant χημειοθεραπεία και φθάνουν στο σημείο οι βλάβες να εξαφανισθούν στις ακτινολογικές εξετάσεις (πλήρης ύφεση), αν και το γεγονός αυτό φαίνεται καλό από πρώτης πλευράς, μελέτες έδειξαν ότι πάνω από το 80% από τις βλάβες αυτές, που ακόμη και κατά το χειρουργείο δεν ανιχνεύονται, περιέχουν βιώσιμο καρκινικό ιστό και αν δεν εξαιρεθούν, φυσικά υποτροπιάζουν. Έτσι λοιπόν, πρέπει και οι βλάβες αυτές να εξαιρούνται και όχι να περιμένουμε οι ασθενείς να υποτροπιάσουν και μετά να τους υποβάλλουμε σε χειρουργική επέμβαση. Η επιβίωση των ασθενών που χειρουργήθηκαν όταν οι όγκοι τους μίκραιναν, αλλά δεν περίμεναν μέχρι να σταματήσει η ύφεση αυτή και να αρχίσει η υποτροπή, είχαν καλύτερη πενταετή επιβίωση (37% έναντι 8%) Συνεπώς η επέμβαση πρέπει να γίνεται όταν είναι εφικτή, κατά τη διάρκεια της neoadjuvant χημειοθεραπείας (downstaging, downsizing) και όχι μετά την ολοκλήρωση κάποιου σχήματος.
Η συμπληρωματική (adjuvant) συστηματική χημειοθεραπεία μετά από ηπατεκτομή για ΜΝΗ από ορθοκολικό καρκίνο δίνεται στην πλειονότητα των ασθενών στις ΗΠΑ αλλά και στην Ελλάδα ως θεραπευτικό σχήμα επιλογής, χωρίς πρακτικά όμως να υπάρχουν προοπτικές μελέτες που να αναδεικνύουν την αξία της, αλλά βασιζόμενοι στα αποτελέσματα της μεθόδου για τον ορθοκολικό καρκίνο καθώς και σε αρκετές ενδείξεις.
Υπάρχουν τρεις αναδρομικές μελέτες, που φαίνεται ότι η μέθοδος ωφελεί τους ασθενείς αυτούς και 2 μικρές προοπτικές, που δεν ευρέθη καμία σημαντική διαφορά στην επιβίωση μεταξύ ασθενών που υπεβλήθησαν σε συμπληρωματική χημειοθεραπεία μετά από ηπατεκτομή συγκριτικά με αυτούς που δεν έλαβαν. Παρόλα αυτά, όμως, φαίνεται ότι η συμπληρωματική χημειοθεραπεία μετά ηπατεκτομή θα συνεχίσει να δίδεται μέχρι αποδείξεως του εναντίου. ίναι φυσικά γνωστό ότι οι ασθενείς που ανταποκρίνονται στη χημειοθεραπεία έχουν καλύτερη πρόγνωση μετά από ηπατεκτομή, αλλά αυτό δεν σημαίνει ότι και αυτοί που δεν ανταποκρίνονται δεν πρέπει να χειρουργούνται, μιας και οι ασθενείς αυτοί εμφανίζουν
καλύτερη επιβίωση από εκείνους που δεν χειρουργούνται (μέχρι και 38% 5ετή επιβίωση). Φυσικά η χημειοθεραπεία δημιουργεί βλάβες στο ήπαρ και ειδικά όταν αυτή χορηγείται ως neoadjuvant, αυτές είναι σημαντικές και περιλαμβάνουν κυρίως τη λιπώδη εκφύλιση αλλά και τη στεατοηπατίτιδα (Irinotecan), καθώς και βλάβες στα ηπατικά κολποειδή (Oxaliplatin).
Περιοχική ηπατική χημειοθεραπεία (HAI)
Η κύρια εστία υποτροπής μετά από ηπατεκτομή είναι όπως ήδη έχει λεχθεί το εναπομείναν ήπαρ (45- 75%). Επειδή το ήπαρ είναι η μόνη εστία της πρώτης υποτροπής στο 40% των ασθενών, η περιοχική ηπατική χημειοθεραπεία είναι η πλέον μελετημένη μέθοδος χορήγησης συμπληρωματικής χημειοθεραπείας μετά από ηπατεκτομή.
Η λογική πίσω από την περιοχική ενδαρτηριακή χημειοθεραπεία του ήπατος ξεκινά, από το γεγονός ότι το σύνολο των όγκων του ήπατος (εκτός από το ΗΚΚ in situ, ή ΗΚΚ <1 cm) λαμβάνουν σχεδόν όλη την αιμάτωσή τους από την ηπατική αρτηρία, αρκετά δε χημειοθεραπευτικά φάρμακα όπως η fluorodeoxyuridine (FUDR) αλλά και άλλα πιο σύγχρονα υφίστανται ηπατική απορρόφηση της τάξης του 90%, πετυχαίνοντας έτσι πολύ υψηλές συγκεντρώσεις στο όργανο, με ασήμαντη συστηματική τοξικότητα. Είναι σαφές ότι η ΗΑΙ είτε μόνη της ή σε συνδυασμό με συστηματική χημειοθεραπεία παρέχει μεγαλύτερη ανταπόκριση συγκριτικά με τη μόνη συστηματική χημειοθεραπεία, όπως αυτή εκφράζεται από τη μικρότερη υποτροπή στο ήπαρ (9% έναντι 36%) και από την καλύτερη 2ετή επιβίωση (86% έναντι 72%).
Τέσσερις μεγάλες προοπτικές μελέτες ενός σκέλους (single-arm trials) και 4 τυφλές προοπτικές μελέτες έχουν εκτενώς μελετήσει τη χρησιμότητα της μεθόδου και δεν υπάρχει σήμερα πλέον καμία αμφιβολία ότι η ΗΑΙ είναι μια πολύ δραστική μέθοδος για τον έλεγχο των ηπατικών μεταστάσεων, σε εξειδικευμένα δε κέντρα αποτελεί τη μέθοδο εκλογής πρόληψης της υποτροπής μετά από ηπατεκτομή για ΜΝΗ από ορθοκολικό καρκίνο και όχι
μόνον. Η σχετική πολυπλοκότητα της μεθόδου την καθιστά να μην είναι ιδιαίτερα ελκυστική στην πλειονότητα των ογκολόγων, πιθανότατα δε εξηγεί την μη έκφραση της αποτελεσματικότητας της θεραπείας σε πολύ μεγαλύτερη επιβίωση σε αρκετές σειρές.
Σε πολλά κέντρα χρησιμοποιείται και η περιοχική χημειοθεραπεία διά της ηπατικής αρτηρίας, μέσω αντλίας (Infusaid) ή καθετήρα με υποδερμάτιο τύμπανο, όπως χρησιμοποιείται και από εμάς, μέθοδος που καλείται περιοχική χημειοθεραπεία διά της ηπατικής αρτηρίας (HAI) (εικόνα). Αρκετές μελέτες δείχνουν ότι ο τρόπος αυτός χημειοθεραπείας σε συνδυασμό πάντα με συστηματική χημειοθεραπεία παρέχει καλύτερα αποτελέσματα από τη μόνο συστηματική σε ανεγχείρητους όγκους και ίσως προσδίδει και καλύτερα αποτελέσματα ως μετεγχειρητική χημειοθεραπεία (μετά ηπατεκτομή για ΜΝΗ) αν και αυτό δεν έχει με βεβαιότητα αποδειχθεί. Πολλοί ογκολόγοι δεν χρησιμοποιούν την ΗΑΙ, μιας και πιστεύουν ότι δεν πλεονεκτεί έναντι της συστηματικής, λόγω κυρίως και των δυσκολιών στη χρήση της αντλίας ή των τυμπάνων των καθετήρων.
Η προσωπική μας άποψη συμφωνεί με αυτών που θέλουν να πιστεύουν ότι η θεραπεία με ΗΑΙ είναι σημαντική, έτσι οι ασθενείς μας που υποβάλλονται σε κολεκτομή για ορθοκολικό καρκίνο με σύγχρονη ΜΝΗ, και αν οι συνθήκες το επιτρέπουν (γενικές και τοπικές), τότε
τοποθετούμε στην πρώτη επέμβαση τον καθετήρα εντός της ηπατικής αρτηρίας μέσω της γαστροδωδεκαδακτυλικής, συνήθως με σύγχρονη εκτέλεση χολοκυστεκτομής για την αποφυγή χημικής οξείας χολοκυστίτιδας κατά τη διάρκεια της χημειοθεραπείας.
Η εφαρμογή της ΗΑΙ στους ασθενείς αυτούς χρησιμοποιείται για χημειοθεραπεία είτε ως neoadjuvant είτε ως παρηγορική χημειοθεραπεία, μιας και αυτό που οι ογκολόγοι θεωρούν πλήρη ανταπόκριση (complete response) πρακτικά δεν υφίσταται. H προσωπική μας εμπειρία στο πρωτόκολλο, που για αρκετά χρόνια εφαρμόζεται στο νοσοκομείο μας (ΠΓΝΑ «ΛΑΪΚΟ») είναι ότι μια μικρή ομάδα ασθενών μπορεί να καταστούν χειρουργήσιμοι
(υποψήφιοι για R0 ηπατεκτομή) και μία άλλη μεγάλη ομάδα θα χρησιμοποιήσουν τη μέθοδο μέχρι το τέλος της ζωής τους, μιας και διαθέτουμε ανέκδοτες προσωπικές περιπτώσεις ασθενών που υπερέβησαν τα 5 έτη με την ανωτέρω μέθοδο (εικόνα 18).
Σήμερα, ο καθετήρας αυτός μπορεί να εισαχθεί με επεμβατικές ακτινολογικές τεχνικές.
Εικόνα 18: Σύγχρονη εκτέλεση ηπατεκτομής και τοποθέτηση καθετήρος στην ΗΑ για περιοχική HAI
Άλλες θεραπείες
Άλλου είδους θεραπείες όπως o TACE (5-FU, mitomycin C, lipiodol, και gelatin foam), ο χημειοεμβολισμός της πυλαίας φλέβας και ακολούθως ηπατεκτομή (neoadjuvant θεραπεία), η καταστροφή με laser, η ανοσοθεραπεία, η χρονοθεραπεία, η απομονωμένη ηπατική έγχυση (Isolated hepatic perfusion) κ.λπ. ευρίσκονται υπό μελέτη, αλλά δεν φαίνεται να ξεπερνούν την αποτελεσματικότητα των προαναφερθεισών ειδών θεραπείας. Ειδικά η ανοσοθεραπεία χρησιμοποιείται κυρίως σε προχωρημένες καταστάσεις, αφού οι άλλες μέθοδοι έχουν αποτύχει. Συνίσταται σε χορήγηση Levamisole, που είναι ένας ανοσοδιεγέρτης, σε συνδυασμό με 5-FU και ένα δραστικό μονοκλωνικό αντίσωμα.
Η εκλεκτική εσωτερική ακτινοθεραπεία (Selective Internal Radiotherapy) επιτρέπει τη χορήγηση υψηλών δόσεων στο ήπαρ (200-300 Gy), που δεν είναι δυνατόν αν χορηγηθούν με την κλασική ακτινοθεραπεία, μιας και το όργανο είναι ακτινοευαίσθητο. Συνίσταται στη χορήγηση μιας δόσης μικροσφαιριδίων (resin ή glass) στην ηπατική αρτηρία (2.0-3.0 Gbq of 90-yttrium) και στην εκλεκτική πρόσληψη, κυρίως από τον όγκο, με ικανοποιητικά αποτελέσματα, περίπου ίδια με αυτά της σημερινής χημειοθεραπείας.
Τελευταία γίνεται λόγος, για μια μέθοδο που ονομάζεται επαναλαμβανόμενος ηπατικός αρτηριακός αποκλεισμός (Repeated hepatic dearterialization) σε συνδυασμό ή όχι με ΗΑΙ, τα δε αποτελέσματα ήταν απογοητευτικά για τη ΜΝΗ από ορθοκολικό καρκίνο, αλλά ικανοποιητικά για ανεγχείρητο ΜΝΗ από καρκίνο στομάχου (ανταπόκριση 70%).
Θεραπευτικές τεχνικές καταστροφής της ΜΝΗ
Η θερμική καταστροφή με εναλλασσόμενο ηλεκτρικό ρεύμα στο φάσμα των ραδιοσυχνοτήτων, ή όπως ονομάζεται διεθνώς Radiofrequency Ablation (RFA), είναι αυτή την περίοδο η δημοφιλέστερη μέθοδος θερμικής καταστροφής. Μια ποικιλία όμως άλλων μεθόδων θερμικής καταστροφής έχει εφαρμοστεί στη ΜΝΗ από ορθοκολικό καρκίνο, όπως το high-intensity focused ultrasound (HIFU), η θερμοθεραπεία με λέιζερ, η εσωτερική
ραδιοθεραπεία με εμφυτεύματα yttrium-90, και πιο πρόσφατα η θερμική καταστροφή με μικροκύματα (MWA) που κερδίζει έδαφος σε δημοτικότητα. Όπως φαίνεται, όλες αυτές οι συσκευές και μέθοδοι εμφανίζουν δημοτικότητα, λίγοι συγγραφείς όμως αναφέρονται για την πραγματική τους αξία, που θα έπρεπε να είναι η αποτελεσματική προσφορά τους στην επιβίωση των ασθενών.
Κρυοθεραπεία
Η τεχνική αυτή στηρίζεται στην καταστροφή καθορισμένης περιοχής μέσα στο ήπαρ με πάγωμα/ ξεπάγωμα, χρησιμοποιώντας στειλεούς που ψύχονται με υγρό άζωτο ή αέριο αργό σε θερμοκρασίες υπό το μηδέν, πλην όμως σήμερα σε λίγα μόνο κέντρα χρησιμοποιείται.
Εικόνα 19: Διεγχειρητική απεικόνιση εφαρμογής Cryotherapy
RFA (Radio Frequency Ablation)
Το RFA, μια τεχνολογία που παρόλο που εξελίσσεται από τις αρχές του 19ου αιώνα, μόνο σήμερα έχει καταφέρει να γίνει μια αποτελεσματική τοπική θεραπεία, με την οποία είναι δυνατόν να καταστραφούν μεταστάσεις με σχετικά λίγες επιπλοκές. Η μέθοδος μπορεί να πραγματοποιηθεί διαδερμικά ή διεγχειρητικά (λαπαροσκοπικά ή ανοικτά) ανάλογα των περιστάσεων, έχει δε πολύ μεγαλύτερη πιθανότητα υποτροπής από την ηπατεκτομή, ενώ
μπορεί να χρησιμοποιηθεί σε συνδυασμό με αυτή (εικόνα 20).
Εικόνα 20: Εγχειρητική εφαρμογή RFA Ablation στο δεξιό λοβό του ήπατος, σε ασθενή με πολλαπλές μεταστατικές εντοπίσεις από ορθοκολικό καρκίνο. Στον ασθενή έχει ήδη διενεργηθεί αριστερή πλάγια ηπατεκτομή, σφηνοειδή εκτομή επιφανειακής μεταστατικής εστίας και τοποθέτηση καθετήρα για στοχευμένη ενδαρτηριακή χημειοθεραπεία.
Η RFA παριστά εντοπισμένη εφαρμογή αγώγιμης θερμικής ενέργειας επί του όγκου για να καταστρέψει τα καρκινικά κύτταρα. Συγκεκριμένα, εναλλασσόμενο ηλεκτρικό ρεύμα με συχνότητα στο φάσμα των ραδιοσυχνοτήτων (συνήθως 460 kHz, αλλά και ανάλογα με την κατασκευάστρια εταιρεία 100-500 kHz) εφαρμόζεται από μια γεννήτρια μέσω ενός ηλεκτροδίου-βελόνης, που τοποθετείται άμεσα στον όγκο. Δεδομένου ότι η θερμοκρασία εντός του όγκου ανυψώνεται πέρα από τους 50-600C, οι πρωτεΐνες μετουσιώνονται, τα κύτταρα καταστρέφονται, και μια ζώνη νέκρωσης που περιβάλλει το ηλεκτρόδιο αναπτύσσεται. Η ύπαρξη πλούσιας πυλαίας κυκλοφορίας στο ήπαρ προστατεύει το ηπατικό παρέγχυμα από βλάβες πέραν των δυνατοτήτων της βελόνας, η δε εφαρμογή χειρισμού Pringle κατά την ώρα της εφαρμογής του RFA δημιουργεί μεγαλύτερες βλάβες από αυτές που αναμένονται.
Διάφορα σχέδια ηλεκτροδίων είναι διαθέσιμα. Όγκοι >4 cm μέγιστης διαμέτρου μπορεί να καταστραφούν με την τοποθέτηση ενός ή πολλών ηλεκτροδίων, που δημιουργούν ένα σφαιρικό έγκαυμα μέχρι 5 – 6 cm διαμέτρου. Μεγαλύτεροι όγκοι απαιτούν πολλαπλές εισαγωγές/συνεδρίες του ηλεκτροδίου-βελόνης. Η μέθοδος πρέπει να προγραμματιστεί, έτσι ώστε οι ζώνες της πηκτικής νέκρωσης να επικαλύπτονται, για να εξασφαλιστεί πλήρης καταστροφή του όγκου, γεγονός όμως τεχνικά δύσκολο. Ιδανικά, μια θερμική ζώνη καταστροφής υγιούς ηπατικού παρεγχύματος πέραν του όγκου πλάτους 1 cm πρέπει να δημιουργηθεί, για να εξασφαλιστεί η καταστροφή του σε υγιή όρια. Όγκοι που καταλήγουν σε σημαντικό αγγειακό σχηματισμό μπορούν να καταστραφούν ακίνδυνα, μιας και το αίμα μέσα στα αγγεία αυτά απάγει τη θερμότητα και έτσι προστατεύεται το αγγειακό ενδοθήλιο («heat sink φαινόμενο»), επιτρέποντας την πλήρη πηκτική νέκρωση του ιστού που περιβάλλει το αγγείο. Γενικώς, όμως, αποφεύγεται η εφαρμογή του RFA πολύ κοντά σε αγγειακές δομές, όπως η ηπατική πύλη ή η κάτω κοίλη φλέβα και οι ηπατικές φλέβες και ειδικά κοντά σε χολαγγεία, τα οποία εύκολα μπορεί να καταστραφούν, με συνέπεια επιπλοκές όπως χοληφόρα συρίγγια, αποστήματα, χολώματα κ.λπ.
Η RFA μπορεί να εφαρμοστεί διαδερμικά, λαπαροσκοπικά ή με ανοικτή χειρουργική επέμβαση. Η διαδερμική προσέγγιση είναι η λιγότερο επεμβατική μπορεί δε να γίνει και με τον ασθενή σε εξωτερική βάση. Το μειονέκτημα της προσέγγισης αυτής είναι η σχετικά κατώτερη δυνατότητα να ανιχνευθεί και να στοχευθεί ένας μικρός όγκος συγκριτικά με το ανοικτό RFA, που καθοδηγείται από IOUS. Επίσης, μερικές θέσεις μέσα στο ήπαρ είναι διαδερμικά απρόσιτες ή συνοδεύονται με υψηλό ποσοστό θερμικού τραυματισμού παρακειμένων οργάνων, όταν χρησιμοποιείται η διαδερμική οδός. Η λαπαροσκοπική RFA προσπέλαση αντιπροσωπεύει μια ελάχιστα επεμβατική μέθοδο, που επιτρέπει την καλύτερη σταδιοποίηση με IOUS απεικόνιση, και με αυτόν τον τρόπο, αποφυγή των παρακειμένων σπλαγχνικών δομών. Όμως μπορεί να είναι τεχνικά δύσκολη, ανάλογα με την ανατομική θέση της μετάστασης.
Η ανοικτή RFA προσπέλαση είναι η πιο επεμβατική μέθοδος, αλλά ίσως η αποτελεσματικότερη. Παρέχει την καλύτερη απεικόνιση και στοχοθέτηση, μιας και δίδεται η ευκαιρία να κινητοποιηθεί πλήρως το ήπαρ, να απομακρύνονται τα παρακείμενα σπλάγχνα, και επίσης μπορεί να χρησιμοποιηθεί ο αγγειακός αποκλεισμός της πύλης του ήπατος (χειρισμός Pringle) εάν είναι απαραίτητο, για εξάλειψη του φαινομένου heat sink και έτσι επαύξηση του θερμικού αποτελέσματος.
Εντός 2 εβδομάδων από την επέμβαση, ΑΤ ή MRI ενδείκνυται να εκτελεσθεί για τον έλεγχο αν ο ιστός στον οποίο έγινε RFA έχει πραγματικά όλος νεκρωθεί. Αν όχι (πρόσληψη σκιαγραφικού στην αρτηριακή φάση), τότε η συνεδρία πρέπει να επαναληφθεί. Τρεις μήνες μετά τη συνεδρία πρέπει πάλι να γίνει μια ΑΤ ή MRI και να συγκριθεί με την προεγχειρητική εικόνα. Το αποτέλεσμα που αναμένεται να ληφθεί είναι μια ομοιογενής μάζα μεγαλύτερη από την προεγχειρητική εστία, ίδια, ή μικρότερη σε μέγεθος από αυτή της 1ης μετεγχειρητικής ΑΤ ή MRI. Το επιθυμητό αποτέλεσμα είναι φυσικά να μην προσλαμβάνει σκιαγραφικό υλικό και να μην είναι μεγαλύτερη σε μέγεθος. Επί οποιασδήποτε αμφιβολίας, τότε η συνεδρία πρέπει να επαναλαμβάνεται.
Μπορεί να συνοδεύεται με άλλες σύγχρονες επεμβάσεις, όπως ηπατεκτομή. Η ανοικτή μέθοδος γενικά προτιμάται σε ασθενείς με πολλαπλούς όγκους, μεταστατικές εστίες σε δύσκολες θέσεις, που δεν μπορεί να προσεγγισθούν με άλλες μεθόδους, ή εάν ο όγκος καταλήγει σε μια σημαντική δομή που πρέπει να μην τραυματιστεί.
Η θεραπεία είναι πολύ αποτελεσματική για μικρές μεταστάσεις <3 cm, όπως και σε αυτή του ΗΚΚ. H συσσωρευμένη μέχρι σήμερα εμπειρία με τη μέθοδο RFA, είναι ικανοποιητική, και μας επιτρέπει να υποστηρίζουμε, ότι αυτή είναι πολύ χρήσιμη στην καταστροφή ηπατικών μεταστάσεων, που χωρίς αυτή θα κρίνονταν ανεγχείρητες. Έτσι, σήμερα, σε ανεγχείρητες καταστάσεις μπορούν να συνδυασθούν οι θερμικές μέθοδοι Έτσι, σήμερα, σε
ανεγχείρητες καταστάσεις μπορούν να συνδυασθούν οι θερμικές μέθοδοι καταστροφής και ειδικά το RFA με την ηπατεκτομή ή και με PVE και δύο σταδίων ηπατεκτομή, για να μπορούν να χειρουργηθούν ασθενείς που τα προηγούμενα χρόνια θεωρούνταν ανεγχείρητοι. Παρόλα αυτά και με αυτή τη μέθοδο, η εξαιρεσιμότητα δεν υπερβαίνει το 30%.
Όμως, η RFA μέθοδος δεν είναι υποκατάστατο της χειρουργικής θεραπείας όπως νόμισαν πολλοί αδικαιολόγητα, γιατί μελέτες απέδειξαν αυτό που υποστηρίζαμε από την αρχή, ότι η υποτροπή του όγκου μετά από το RFA είναι πολύ υψηλή. Έτσι οι μέχρι σήμερα δημοσιευμένες μεταναλύσεις ανέδειξαν το πρόβλημα της χρήσης της μεθόδου σε μαζική κλίμακα από μη χειρουργούς ήπατος με πτωχά απώτερα αποτελέσματα και έθεσαν
πρακτικά και τις ενδείξεις της μεθόδου, που είναι οι μεταστάσεις και γενικά οι όγκοι που είναι ανεγχείρητοι, πάντα δε στα πλαίσια ενός χάρτη προς θεραπεία των ασθενών, που πριν δεν μπορούσαν να χειρουργηθούν.
Σε επιλεγμένους ασθενείς με αρχικά ανεγχείρητες πολλαπλές και αμφωτερόπλευρες μεταστάσεις ήπατος (MBCLM), ο συνδυασμός ηπατεκτομής 2 σταδίων (TSHP) με αυτόν του αποκλεισμού της πυλαίας φλέβας (PVE) και πολλές φορές με τη χρήση του RFA μπορεί να γίνει με ασφάλεια και να επιτευχθεί μακρά επιβίωση, παρόμοια με αυτή που επιτυγχάνεται σε ασθενείς με χειρουργήσιμη νόσο του ήπατος.
Η RFA δεν πρέπει να θεωρείται ως μέθοδος αντικατάστασης της ηπατεκτομής, αλλά ως συμπλήρωμα ή επέκταση της εντοπισμένης θεραπείας σε ανεγχείρητους ασθενείς.
Ασθενείς με εξαιρέσιμη ΜΝΗ από ορθοκολικό καρκίνο πρέπει να υποβάλλονται σε ηπατεκτομή και όχι σε RFA. Η κύρια ένδειξη του RFA είναι στους ασθενείς που δεν ικανοποιούν τα κριτήρια εξαιρεσιμότητας (ανατομικά ή άλλα), αλλά είναι υποψήφιοι για τοπική θεραπεία στο ήπαρ, μιας και έχουν νόσο εντοπιζόμενη μόνον στο όργανο αυτό.
Τέτοια παραδείγματα είναι, όταν ένας αριθμός μεταστάσεων υφίσταται π.χ. στο δεξιό λοβό και ένας μικρότερος στον αριστερό λοβό του ήπατος, η δε ηπατεκτομή θα οδηγήσει σε ανεπαρκή εναπομείναντα ηπατικό ιστό, τότε εκτελείται δεξιά ηπατεκτομή και RFA στις βλάβες του αριστερού λοβού καθώς και πολλοί άλλοι τέτοιοι συνδυασμοί.
Ο συνδυασμός της ηπατεκτομής με RFA μεγαλώνει τον αριθμό των ασθενών που μπορεί να καταστούν υποψήφιοι για χειρουργική θεραπεία, ιδιαίτερα δε όταν μεγάλες μεταστάσεις είναι δυνατόν να εξαιρεθούν και οι μικρότερες να καταστραφούν με RFA. Η προσθήκη του RFA στην ηπατεκτομή δεν αλλάζει τη νοσηρότητα και τη θνητότητα των ασθενών, συγκριτικά με αυτούς που υπέστησαν μόνον ηπατεκτομή. Οι επιπλοκές μετά RFA είναι
σχετικά σπάνιες και λιγότερες από 10%, περιλαμβάνουν δε: πυρετό, άλγος, χολικά συρίγγια, χολώματα, περιηπατικά αποστήματα, ηπατική ανεπάρκεια, τραύματα ηπατικής αρτηρίας, εγκαύματα δέρματος και διαφράγματος, πλευριτικές συλλογές, αιμορραγική διάθεση και κοιλιακή ταχυκαρδία. Η αιμορραγία είναι σπάνια επιπλοκή της μεθόδου, μιας και ένα από τα πλεονεκτήματά της είναι η αιμόσταση. Μετά από την καταστροφή μιας βλάβης, η βελόνη αποσύρεται αργά εν λειτουργία και η διαδρομή της καταστρέφεται. Με τη μέθοδο αυτή σπάνια παρατηρείται αιμορραγία, την δε ιδιότητα αυτή χρησιμοποιούμε στην επονομαζόμενη RFA υποβοηθούμενη ηπατεκτομή. Η θνητότητα της μεθόδου είναι πολύ χαμηλή (0,5%) και φυσικά η ανοικτή μέθοδος ενέχει μεγαλύτερη νοσηρότητα από τη διαδερμική.
Υποτροπή της νόσου ή εμμονή της μεταστατικής πάθησης στην περιοχή του RFA έχει αναφερθεί ότι είναι λιγότερη από 10% μετά από ανοικτό RFA, συγκριτικά με το διαδερμικό που είναι μέχρι και 40%. H τοπική υποτροπή μετά από RFA είναι ιδιαίτερα εξαρτώμενη από το μέγεθος και τη θέση των όγκων μέσα, στο ήπαρ. Οι περισσότερες αποτυχίες εμφανίζονται στους μεγάλους όγκους (μεγαλύτερους από 5.0 cm). H ενδοηπατική υποτροπή σε μικρούς όγκους (<3 cm) είναι σχετικά ασυνήθιστη (3,6%) συγκριτικά με αυτούς >5 cm (50%) (εικόνα 21).
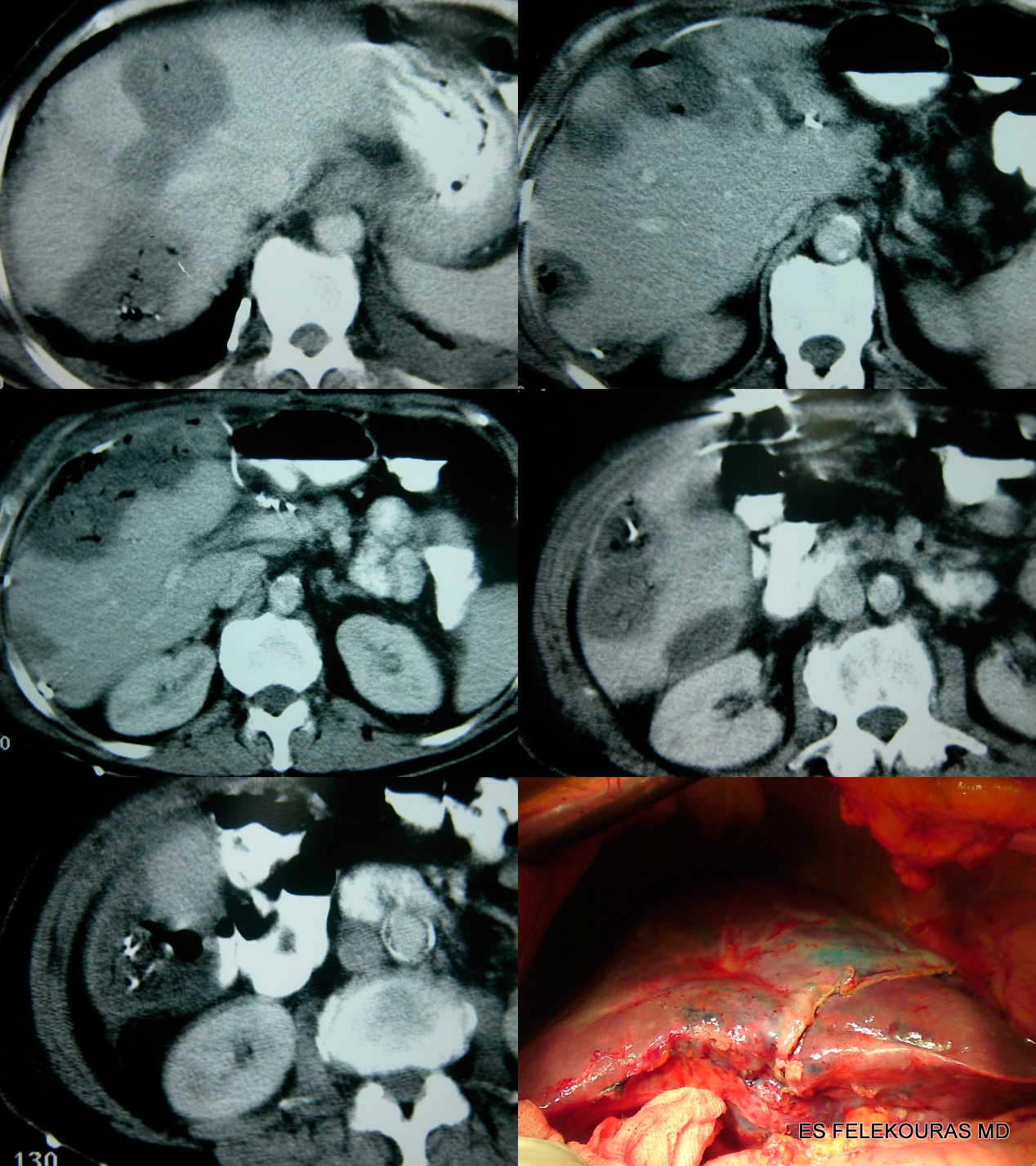
Εικόνα 21: Α. Σε ΑT απεικόνιση υποτροπής, στα πλαίσια του follow up μετά από διαδερμικό RFA Ablation για ΜΝΗ από ορθοκολικό καρκίνο. Β και Γ. Διεγχειρητική απεικόνιση διτμηματεκτομής στον ίδιο ασθενή.
Η επιβίωση μετά από RFA είναι δύσκολο να ερμηνευθεί, μιας και πολλοί ασθενείς που υποβάλλονται στη θεραπεία αυτή χαρακτηρίζονται από πολλούς πτωχούς προγνωστικούς παράγοντες (π.χ. ανεγχείρητη νόσο, πολλαπλούς όγκους, αμφωτερόπλευρη νόσο κ.λπ.), κάνοντας σύγκριση με τους ασθενείς που έχουν υποβληθεί σε δύσκολη ηπατεκτομή. Γενικά, μελέτες με μόνο RFA προσδίδουν μια διάμεση επιβίωση περίπου μέχρι σήμερα
δημοσιευμένες μεταναλύσεις δεν έχουν δείξει όφελος από τη χρήση του RFA, εκτός ίσως από τις μικρές <3 cm μεταστατικές βλάβες και στο μικρό (<3 cm) HKΚ. Σε μια πρόσφατη μελέτη, η σύγκριση της υποτροπής και της έκβασης μετά από ηπατεκτομή, RFA, και συνδυασμένη ηπατεκτομή και RFA για ΜΝΗ από ορθοκολικό καρκίνο απέδειξε ότι η επιβίωση ελεύθερης νόσου και η συνολική επιβίωση ήταν σημαντικά χειρότερες για τους ασθενείς με RFA. Αν και η επιλογή των ασθενών για RFA μπορεί να επηρέασε τα αποτελέσματα της μελέτης, αυτή εν τούτοις δίνει έμφαση στο ότι πριν η RFA θερμική καταστροφή γίνει αποδεκτή ως εναλλακτική της ηπατεκτομής λύση ή απορριφθεί τελείως για τη ΜΝΗ από ορθοκολικό καρκίνο, είναι απαραίτητο να γίνουν τυχαιοποιημένες διπλές τυφλές μελέτες που να συγκρίνουν τη μέθοδο με την ηπατεκτομή. Μια τέτοια μελέτη έδειξε ότι η RFA δεν είναι εναλλακτική της ηπατεκτομής λύση, μιας και η επιβίωση των «ανεγχείρητων» ασθενών που υπεβλήθησαν σε ηπατεκτομή και RFA ή μόνον RFA ήταν καλύτερη σε ασθενείς που υπεβλήθη σαν μόνο σε χημειοθεραπεία.
Εικόνα 22: Ασθενής με πολλές βλάβες ήπατος από ΜΝΗ που κρίθηκε μη εξαιρέσιμη και υπεβλήθει σε μαζικά RFA των βλαβών. Η επιβίωση του ήταν 5 έτη με συνοδό περιοδική χημειοθεραπεία
Μικροκύματα
Μια σχετικά νέα και αναδυόμενη τεχνική θερμικής καταστροφής περιλαμβάνει τη χρήση μικροκυμάτων (MWA). Η μέθοδος προσφέρει διάφορα πλεονεκτήματα συγκριτικά με το RFA, συμπεριλαμβανομένης της ταχύτητας διάδοσης της ενέργειας και ίσως της δυνατότητας να παραχθεί μια ευρύτερη ζώνη καταστροφής. Η ικανότητα του μικροκύματος να παράγει μεγαλύτερες ζώνες θερμότητας συσχετίζεται πιθανώς με το γεγονός ότι,
αντίθετα από RFA, η ενέργεια των μικροκυμάτων δεν φαίνεται να περιορίζεται από την απανθράκωση και την ιστική αφυδάτωση. Μέχρι σήμερα, η εμπειρία με τη μέθοδο αυτή είναι περιορισμένη, πρόσθετες δε μελέτες είναι απαραίτητες πριν από την καθιέρωσή της σε ευρεία βάση.
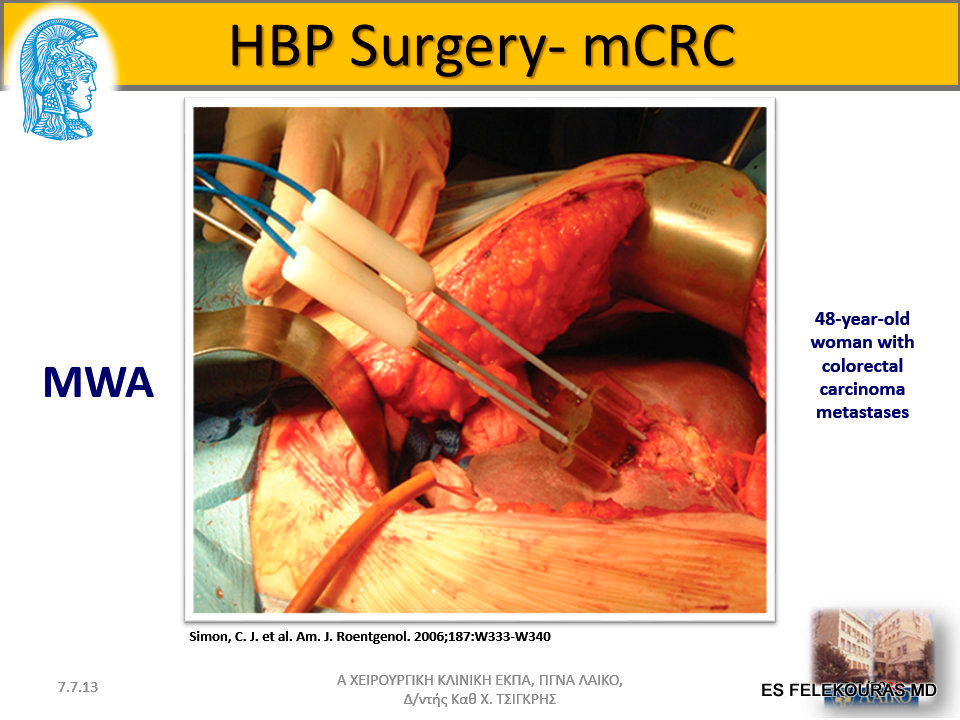
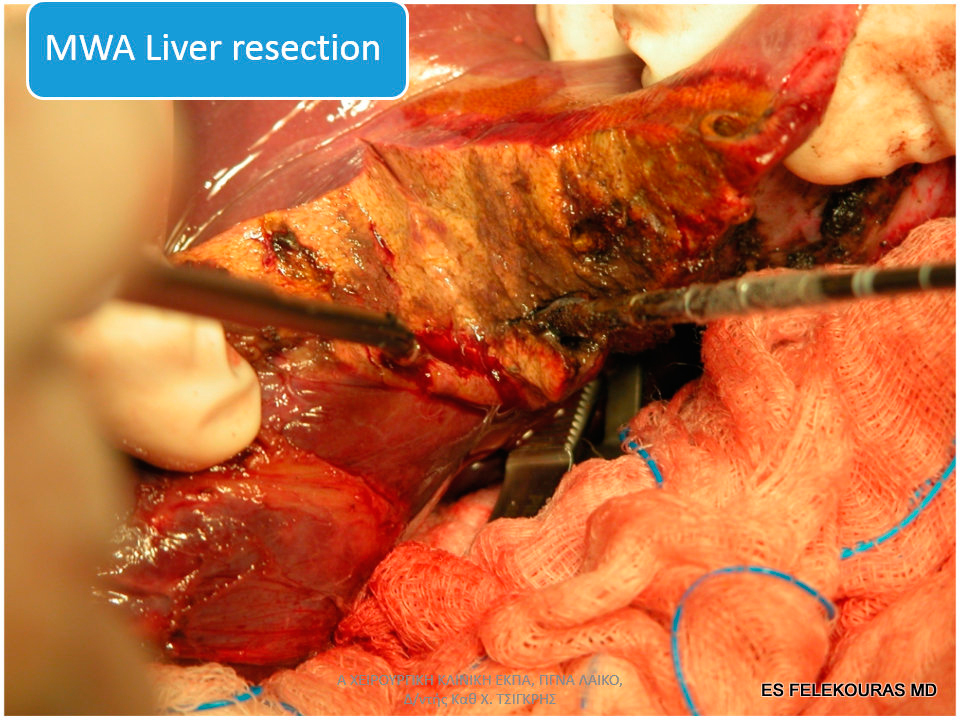
Εικόνα 23: Επάνω διεγχειρητικό MWA, Κάτω MWA υποβοηθουμένη ηπατεκτομή για ΜΝΗ
Συμπέρασμα
Εκείνο που έχει ιδιαίτερη σημασία στη θεραπεία της ΜΝΗ εκ του παχέος εντέρου είναι ότι: η χειρουργική θεραπεία και όχι η χημειοθεραπεία ή το RFA, συνιστά τη θεραπεία εκλογής στους ασθενείς με εξαιρέσιμη νόσο · ο συνδυασμός, πολλές φορές, πολλών τεχνικών και ειδών θεραπείας είναι απαραίτητος για την αντιμετώπιση των όγκων αυτών, και · οι ασθενείς με ΜΝΗ εκ του παχέος εντέρου θα πρέπει να παρακολουθούνται συστηματικά
από χειρουργό ήπατος, που είναι ο μόνος ικανός να αξιολογήσει την πιθανότητα χειρουργικής θεραπείας της νόσου και έτσι να επιτευχθεί το καλύτερο προσδοκώμενο αποτέλεσμα. Η επιβίωση ασθενών με ΜΝΗ από ορθοκολικό καρκίνο σήμερα έχει αλλάξει, θεωρούμε δε ότι σε όλους τους ασθενείς πρέπει να δίνεται το δικαίωμα της επέμβασης σε συνδυασμό με κάθε μέθοδο που μπορεί να βελτιώσει τη μακρά επιβίωσή τους. Έτσι,
σήμερα, μεγάλες μελέτες έχουν δείξει ότι οι ασθενείς με ΜΝΗ από το παχύ έντερο που υποβάλλονται σε R0 ηπατεκτομή ως κύρια μέθοδο θεραπείας της, εμφανίζουν 5ετή και 10ετή επιβίωση πολλές φορές πάνω από 20%.
Η υποτροπή της νόσου μετά την ηπατεκτομή επισυμβαίνει σε 2 περίπου έτη στα 2/3 των ασθενών, η δε ίαση θεωρείται πιθανή όταν ο όγκος δεν έχει υποτροπιάσει μετά από 7 έτη.
Η υποτροπή επισυμβαίνει μόνο στο εναπομείναν ήπαρ στο 40-50% περίπου και στους πνεύμονες στο 20% των ασθενών. Η πιθανότητα υποτροπής σε οποιοδήποτε όργανο είναι 65% στα 5 έτη.
Ένα 20% αυτών με υποτροπή μπορεί να υποβληθούν σε επανηπατεκτομή μία ή και περισσότερες φορές με πολύ καλά αποτελέσματα. Η πενταετής επιβίωση σε τέτοιες περιπτώσεις είναι συνήθως 30-40% (από 16-74%). Επειδή η ως άνω αναφερόμενη πιθανότητα είναι σημαντική, οι ασθενείς μετά από την πρώτη ηπατεκτομή πρέπει να παρακολουθούνται στενά με τακτικό έλεγχο CEA και με απεικονιστικές εξετάσεις (κυρίως ΑΤ), έτσι ώστε η πιθανή υποτροπή να ανιχνευτεί έγκαιρα σε όσο το δυνατόν πρωιμότερο στάδιο.
Όπως έχει ήδη αναφερθεί, ασθενείς που δεν είναι υποψήφιοι για ηπατεκτομή εμφανίζουν πολύ μικρή 5ετή επιβίωση και αντίστοιχη μηδενική 10ετή. Σε αντίθεση, σε ασθενείς με ηπατεκτομή και μακρά παρακολούθηση, απεδείχθη 10ετής επιβίωση 22-24% και αντίστοιχη γύρω στο 20% πέραν των 15-20 ετών. Η ΜΝΗ από ορθοκολικό καρκίνο έχει κακή πρόγνωση με συστηματική χημειοθεραπεία ή καμία θεραπεία. Η R0 ηπατεκτομή είναι η θεραπεία εκλογής επί απουσίας εξωηπατικής νόσου, μπορεί δε να επιτύχει μακρόχρονη απώτερη επιβίωση σε άνω από το 1/3 των ασθενών αυτών και 5ετή γύρω στο 40%-58%.
Στα τελευταία 10 χρόνια τα κριτήρια εξαιρεσιμότητας έχουν αλλάξει, εξαιρέσιμη δε θεωρείται η νόσος που μετά την αφαίρεσή της παραμένει στον ασθενή ικανοποιητικός ιστός ήπατος, ενώ φυσικά η εξαίρεση γίνεται επί αρνητικών ορίων (R0) και για την επίτευξη του στόχου αυτού πρέπει να χρησιμοποιηθεί κάθε μέσο που διαθέτουμε, όπως PVE, ηπατεκτομή 2 σταδίων, προεγχειρητική χημειοθεραπεία, RFA κ.λπ. Τα κριτήρια αυτά έχουν
επεκταθεί ακόμα περισσότερο, ώστε να περιλάβουν και ασθενείς με ενδοηπατική και εξωηπατική νόσο. Η θεραπεία των ασθενών αυτών είναι περίπλοκη, πρέπει δε να καθορίζεται από ομάδα ειδικευμένων ιατρών με ανάλογους χειρισμούς. Από την άλλη πλευρά η έρευνα προχωρά και η προσπάθεια για την ανεύρεση νέων και πιο στοχευμένων χημειοθεραπευτικών παραγόντων συνεχίζεται, με στόχο τη βελτίωση του προσδόκιμου της
ζωής όλων των ασθενών αυτών.
Τέλος, θα πρέπει να τονισθεί ότι θεωρούμε το νόσημα ως μείζον, μιας και μεγάλο ποσοστό ασθενών στην καθ’ ημέρα πράξη ενός χειρουργού είναι ασθενείς με ΜΝΗ από ορθοκολικό καρκίνο και άλλες πρωτοπαθείς κακοήθειες. Η ΜΝΗ από ορθοκολικό καρκίνο και η αντιμετώπισή της είναι ο δρόμος για την κατανόηση και αντιμετώπιση της ΜΝΗ από όλες τις εστίες στο μέλλον.
Εμείς πιστεύουμε ότι τα αποτελέσματα μας είναι ανάλογα των διεθνών κέντρων και περιμένουμε περαιτέρω βελτίωση της επιβίωσης των ασθενών μας (εικόνα).
Εικόνα 24: Αποτελέσματα σε επιβίωσης στο κέντρο μας (αριστερά, actuarial survival) σε αντιπαραβολή με τα διεθνώς κείμενα (δεξιά)